Ph щелочи и кислоты: Кислоты, основания, pH и буферные растворы (статья)
Уровень pH: Щелочные, кислотные и нейтральные препараты
В современной парикмахерской среде нередко обсуждается такое понятие, как pH косметического продукта. Мастера задают вопросы коллегам и технологам брендов, но получить вразумительный ответ удается далеко не всегда. В этой статье вы узнаете всю необходимую информацию по этому вопросу и научитесь применять ее в вашей работе.
Что такое уровень pH (водородный показатель)?
В химии водородный показатель (pH уровень) является мерой кислотности или щелочности (основности) в водном растворе. Без воды в составе нельзя измерять pH, поэтому не бывает pH показателей таких косметических средств как: жидкие кристаллы, масла, лаки для волос (там где нет воды в составе. Аналогичная ситуация и с осветляющими порошками (правда только пока они находятся в сухом виде, так как если добавить в него окислитель, где содержится вода, то уже этой смеси измерить pH можно).
Величина pH измеряется в пределах от 0 до 14. Чистая дистиллированная вода при температуре 25 °C считается нейтральной. Растворы же с уровнем pH ниже 7 — кислые, а выше 7 — щелочные. Хотя на вид эти цифры не сильно различаются, надо понимать, что уровень pH имеет логарифмическую шкалу и поэтому реальная разница — это 10 в степени равной разнице между значениями. Так например разница между pH 3,5 и pH 5,5 — означает, что продукт с pH 3,5 в 100 раз кислее, чем второй показатель (10 во второй степени). Аналогично и со щелочностью, если сравнивать pH 7 и 10, то продукт с pH 10 в 1000 раз более щелочной, чем нейтральный с pH 7.
Растворы же с уровнем pH ниже 7 — кислые, а выше 7 — щелочные. Хотя на вид эти цифры не сильно различаются, надо понимать, что уровень pH имеет логарифмическую шкалу и поэтому реальная разница — это 10 в степени равной разнице между значениями. Так например разница между pH 3,5 и pH 5,5 — означает, что продукт с pH 3,5 в 100 раз кислее, чем второй показатель (10 во второй степени). Аналогично и со щелочностью, если сравнивать pH 7 и 10, то продукт с pH 10 в 1000 раз более щелочной, чем нейтральный с pH 7.
Волосы на растворы разных pH реагируют по разному. В кислых средах (но не экстремально кислых, при которых уже даже белок разъедается) кутикульный слой волоса старается закрыться (если он есть на волосах, так как в случае поврежденных волос его просто нет, что отчетливо видно на фото в статье о пористости), в щелочных средах — напротив, кутикульный слой разрыхляется и становится пористым, а очень концентрированные щелочи тоже могут разрушать белки волоса и не хуже, чем концентрированные кислоты.
Подробнее о pH воды
В жизни мы в основном встречаемся не с дистиллированной водой, а с водой из водопроводного крана, поэтому уровень pH воды (кислотность воды) зачастую может колебаться в пределах слабокислых — слабощелочных сред. Вода со слабокислым pH подходит для волос. Ее свойства способствуют закрытию кутикулы и поддержанию искусственного цвета волос. Нейтральный pH в принципе не оказывает по губного воздействия на волосы, однако требует уже обязательного применения масок и кондиционеров для волос, чтобы дополнительно стимулировать закрытие кутикулы и поддерживать цвет.
Слабощелочные воды напротив раскрывают кутикульный слой волос и способствуют вымыванию искусственных цветов, а также вызывают тусклость и спутываемость волос. В таком случае без применения кислотных кондиционеров не обойтись, так как природного увлажнения может не хватить для восстановления естественных условий для волос.
При уходе за окрашенными и завитыми волосами стоит поддерживать кислотный pH, так как именно он способствует сохранению цвета и формы волос. Для этого на косметическом рынке существуют специальные серии препаратов максимально подходящие под каждый случай.
Для этого на косметическом рынке существуют специальные серии препаратов максимально подходящие под каждый случай.
Реакция нейтрализации
Кислые и щелочные растворы, равно как чистые кислоты и щелочи — это вещества, которые имеют противоположные характеристики, могут реагировать друг с другом и нейтрализовывать друг друга (гасить). В химии реакция нейтрализации — это реакция между кислотой и щелочным веществом (иначе его еще называют основанием) с образованием соли и воды. Если они равные по силе концентрации, то в результате — мы получаем близкий к нейтральному pH.
Всегда при смешивании в 1 миске или на 1 голове сразу щелочных и кислотных продуктов эта реакция будет протекать и парикмахеры с ней сталкиваются регулярно. Так например все знают, что окислительные эмульсии содержат небольше количество кислоты, которая делает продукт стабильным, а краска содержит щелочь. Когда мы эти два продукта смешиваем в миске, то получаем в первые секунды нейтрализацию. Так как щелочей в краске гораздо больше, чем кислоты в окислителе, то в результате мы получаем состав щелочной, но сама реакция нейтрализации протекает и кислота гасится.
Это активно используют, например, когда после осветляющих сильнощелочных препаратов при смывании наносят кислотные шампунь и кондиционер, что приводит к мягкой нейтрализации остатков щелочей в волосах и восстановлению pH волос и кожи головы до оптимального уровня.
Показатель pH волос
Показатель pH определяется только для водных растворов, но волосы не являются раствором, при этом неоднократно в рекламе можно услышать понятия типа: «pH кожи», «pH волос». О каком показателе тут говорят?
Ответе на этот вопрос достаточно прост. За показатель pH кожи и волос принимают pH природного водно-жирового (гидролипидного) слоя здорового человека, покрывающего кожу и волосы. Фактически это pH кожных выделений, которые вырабатываются кожей и распределяются по длине волос при расчесывании. pH кожи, как и волос, около 5, причем зависит пола, возраста и целого ряда других факторов, включая место на теле человека. К примеру, pH кожи головы – 4-5,5, в то время как показатель в зоне подмышек будет равен 6,5.
Многие заболевания кожи связаны с изменением pH и тогда уже этот уровень не является нормальным. Например, грибковые инфекции приводят к защелачиванию кожных выделений, а псориаз смещает этот показатель наоборот в более кислую сторону.
В косметике обычно оптимальным значением pH кожи головы и волос считают 5-5,5 (ближе к 5,5) и стараются его поддерживать уходом.
pH косметики для волос
Сейчас на рынке есть множество косметических средств и процедур с волосами, которые по разному воздействуют на pH волос. Какие-то препараты смещают уровень pH в щелочную сторону, тем самым нарушая естественные условия и структуру волос, а какие-то препараты, наоборот возвращают кислотную среду, пытаясь нейтрализовать любые пагубные воздействия. Поэтому целесообразно разделить все препараты для работы с волосами на три группы: кислотные, щелочные и нейтральные и рассматривать их отдельно.
Важно! При химических реакциях на волосах составы смесей сильно могут меняться по мере прохождения реакций и pH таких продуктов тоже будет меняться. Например, при осветлении, щелочной состав осветляющего порошка реагирует с перекисью в результате этого образуется вода, летит аммиак (что слышно по запаху) и т.п. При этом очень важно для состава, чтобы показатель pH сильно не падала, так как чрезмерное закисление будет отрицательно влиять на эффективность. Поэтому чтобы pH продукта был стабильным несмотря на химические реакции в осветляющий порошок обязательно добавляют буферные вещества, которые как раз помогают составу удерживать pH продукта в течении всего времени выдержки и гарантированного срока хранения продукта.
Например, при осветлении, щелочной состав осветляющего порошка реагирует с перекисью в результате этого образуется вода, летит аммиак (что слышно по запаху) и т.п. При этом очень важно для состава, чтобы показатель pH сильно не падала, так как чрезмерное закисление будет отрицательно влиять на эффективность. Поэтому чтобы pH продукта был стабильным несмотря на химические реакции в осветляющий порошок обязательно добавляют буферные вещества, которые как раз помогают составу удерживать pH продукта в течении всего времени выдержки и гарантированного срока хранения продукта.
Щелочные препараты для волос
В эту группу входят препараты для окрашивания волос, завивки и выпрямления. Все они имеют два обязательных условия для работы: проникновение во внутрь волоса и проведение внутренних изменений в волосах. Так как в здоровые натуральные волосы очень сложно проникнуть любому препарату, то для раскрытия волоса в эти препараты добавляют щелочные компоненты.
Перманентные (стойкие) краски для волос имеют pH 9-11. Эта величина очень сильно зависит от производителя, а также от степени осветления волос. Наиболее щелочными всегда являются осветляющие ряды красителя, так как им не просто нужно проникнуть в волос, но и произвести очень сильные изменения внутри волоса — осветлить пигмент.
Эта величина очень сильно зависит от производителя, а также от степени осветления волос. Наиболее щелочными всегда являются осветляющие ряды красителя, так как им не просто нужно проникнуть в волос, но и произвести очень сильные изменения внутри волоса — осветлить пигмент.
На том же уровне pH находятся препараты для химической завивки. Их pH колеблется в диапазоне 6,8—9,1 и зависит от типа препарата, а также под какой волос данный препарат рассчитан. Например, завивки которые дают лишь легкую волну (без жестких локонов — «безтиогликолевый тип завивок») имеют более низкий pH, а более сильные по воздействию тиогликолевые завивки — более щелочные.
Современные тиогликолевые препараты для химического выпрямления волос имеют pH на уровне 10 и являются достаточно щадящими, по сравнению со щелочным выпрямлением, которое использовалось еще лет 10 назад и имело pH равное 13.
В отдельные группы препаратов по уровню pH стоит выделить спец-осветляющие красители и деколорирующие кремы и масла. Эта группа из-за сильного осветляющего воздействия, которое от нее требуется, имеет высокий уровень щелочности в районе 10-11.
Эта группа из-за сильного осветляющего воздействия, которое от нее требуется, имеет высокий уровень щелочности в районе 10-11.
Последний препарат в данной группе — осветляющий порошок. Он относится к наиболее щелочной группе препаратов, которая сейчас присутствует на косметическом рынке. pH этой группы в среднем имеет значение 12 (как уже упоминалось — это pH продукта в смеси с окислителем в стандартной пропорции).
Менее щелочными являются тонирующие краски — их pH лежит в диапазоне 8-9. Семипераманентные могут быть как слегка щелочными, так и относиться к кислотным продуктам (все зависит от состава и применяемых пигментов).
По факту все приведенные значения pH — это «средняя температура по больнице», причем не понятно по какому количеству пациентов построенная, так как каждый производитель делает продукты по своим собственным формулам и может несколько менять эти показатели. По этой причине в интернете по этой теме нет единых стандартов, и каждый автор приводит свою собственную усредненную статистику. И всегда можно найти точные значения отдельных брендов, которые могут не попадать в указанные диапазоны. Но в целом приведенные цифры позволяют увидеть как соотносятся по щелочности продукты между собой.
И всегда можно найти точные значения отдельных брендов, которые могут не попадать в указанные диапазоны. Но в целом приведенные цифры позволяют увидеть как соотносятся по щелочности продукты между собой.
Индикаторные полоски меняют свой цвет в зависимости от pH среды в которую погружаются.
Если необходимо узнать значение pH того или иного продукта, вам его может либо дать представитель производителя, либо его нужно будет мерять самому специальными приборами — pH-метрами или индикаторными тест-полосками
Кислотные препараты для волос
В этой группе препаратов находятся практически все средства по уходу за волосами. Это разнообразные маски, кондиционеры, кислотные шампуни, лосьоны и прочее. Задача этих препаратов — ухаживать за волосами и поддерживать их здоровый вид. От них не требуется изменений, противоречащих природе волос, поэтому в щелочах в составе препаратов нет необходимости. Более того смещенный уровень pH после агрессивных процедур необходимо возвращать к природному, поэтому препараты в этой группе все имеют в своем составе кислоты.
Самая обширная подгруппа среди кислотных препаратов — это маски и кондиционеры (бальзамы). Их pH находится в пределах 3,5-6,0 и зависит от назначения препарата. Так, наиболее кислые маски, это те, которые используются после агрессивных парикмахерских процедур, типа осветления. Чуть более в нейтральную сторону маски — это зачастую домашний уход, который наносится просто после мытья головы, а кислотные — салонный (например кислотные кондиционеры после окрашивания волос).
Кислотные шампуни чаще всего встречаются в салонной косметике, но и бытовые кислотные шампуни также не редкость,. Их pH колеблется 4,5-6,5.
Препараты для волос с нейтральным pH
В эту группу стоит отнести препараты, pH которых наиболее близок к нейтральному значению. Сюда стоит отнести временные (физические красители), а также нейтральные и слабощелочные шампуни.
Нейтральная группа шампуней сменила на косметическом рынке своих предшественников — щелочных шампуней (представители которых в профессиональных сериях встречаются все реже и реже). Ведь задача шампуня — хорошо вымыть поверхность волоса, а не почистить его изнутри. Хотя порой можно услышать от всяких гуру, что на нашем рынке почти все шампуни щелочные — это не совсем так, хотя и могло быть правдой лет 10-15 назад.
Ведь задача шампуня — хорошо вымыть поверхность волоса, а не почистить его изнутри. Хотя порой можно услышать от всяких гуру, что на нашем рынке почти все шампуни щелочные — это не совсем так, хотя и могло быть правдой лет 10-15 назад.
Как показывают исследования рынков шампуней в Бразилии 2014 года, опубликованные в Международном журнале трихологии (International Journal of Trichology) — большая часть популярных продуктов на рынке на тот момент, — шампуни с pH в диапазоне 5,5-7 (а именно 88 из 123 протестированных), а в профессиональных сериях основная масса тестируемых продуктов даже находится в диапазоне pH 5-6. На нашем рынке эти показатели могут отличаться, но не кардинально, так как местные производители косметики следять за применяемыми технологиями, как нашими, так и европейскими.
Шампуни с нейтральным pH — это сейчас достаточно дешевый и работающий вариант, по сравнению с кислотными. Их pH находится в пределах 6,5-7,5. Согласно данным бразильских исследователей в этом диапазоне находится примерно 43% от тестированных шампуней. В этой же группе также присутствуют щелочные детские шампуни “без слез”, pH которых находиться в пределах примерно 6,5-7. Данная величина pH считается нормальной для детских продуктов, так как более кислые или щелочные шампуни вызывают раздражение глаз у детей, а следовательно — недопустимы.
В этой же группе также присутствуют щелочные детские шампуни “без слез”, pH которых находиться в пределах примерно 6,5-7. Данная величина pH считается нормальной для детских продуктов, так как более кислые или щелочные шампуни вызывают раздражение глаз у детей, а следовательно — недопустимы.
Последний представитель нейтральной группы — это временный (физический краситель), его pH близка к нейтральному, но все же зачастую смещена в слабо щелочную область и колеблется в пределах 6,5-8. Это связано с тем, что любая краска наиболее эффективно закрепляется только на рыхлой от щелочного воздействия поверхности волоса.
Еще несколько важных моментов
Хотя точные показатели pH того или иного продукта может указать вам только производитель (как вариант еще можно померять самим при наличии соот вующего инструментария), но… в целом зания особенности работы того или иного продукта можно приблизительно понять к какому виду продуктов по pH его стоит отнести и использовать в соответствии с этим. И всегда следует помнить об оптимальном pH для кожи и волос, потому что сильные перегибы по показателю pH в обе стороны будут оказывать негативный эффект на волосы. И при любой работе с косметикой важно стремиться к балансу: после сильного защелачивания применять закисляющий уход, а после сильного закисления и защелачивать хотя бы с помощью обильного смывания составов с волос водой, pH которой все равно более щелочной в сравнении с pH волос и кожи головы.
И всегда следует помнить об оптимальном pH для кожи и волос, потому что сильные перегибы по показателю pH в обе стороны будут оказывать негативный эффект на волосы. И при любой работе с косметикой важно стремиться к балансу: после сильного защелачивания применять закисляющий уход, а после сильного закисления и защелачивать хотя бы с помощью обильного смывания составов с волос водой, pH которой все равно более щелочной в сравнении с pH волос и кожи головы.
Кислота или щелочь — что полезней для человека?
Ответ на этот вопрос, как всегда, звучит примиряюще – важна гармония! Идеальный кислотно-щелочной баланс организма человека нейтральный — pH 7,36. Этот важный показатель, отвечающий за здоровье и долголетие, каждый может измерить в домашних условиях.
Если анализ показал кислотную среду (pH меньше 7,36), значит, что у вас развивается ацидоз, т.е снижается усвоение необходимых организму минералов: калия, кальция, магния, натрия. Последствием дефицита этих важных веществ уже скоро могут стать снижение иммунитета, хрупкость костей, слабость. А потом могут начаться боли в суставах и мышцах, проблемы с сердцем и кровообращением, скачки давления, мочекаменная болезнь и диабет. Также следует знать, что ацидоз предрасполагает к опухолям, в том числе злокачественым.
А потом могут начаться боли в суставах и мышцах, проблемы с сердцем и кровообращением, скачки давления, мочекаменная болезнь и диабет. Также следует знать, что ацидоз предрасполагает к опухолям, в том числе злокачественым.
Если же показатель pH более 8,5, т.е. слишком сдвинут в сторону щелочи, то это тоже непорядок: может начаться дисфункция работы всего ЖКТ, плохое усвоение пищи и дурной запах изо рта. Но главное следствие щелочного сдвига pH вашего организма – захламление крови токсинами. Это состояние приводит к хроническим запорам, проблемам с печенью и, как следствие, к аллергии, невозможности противостоять грибковым заболеваниям и, опять же, склонности к онкологии.
Таким образом, для нормального функционирования организма человека, для правильного течения всех биохимических реакций необходимы и кислоты, и щелочи.
Однако не так давно стали появляться научные теории, в которых «окисление» напрямую связывается со старением организма, а борьба со старением стала приравниваться к борьбе с кислотностью, даже появилось название класса веществ–участников этой борьбы, получивших названием «антиоксиданты».
В основе этих теорий лежат факты: новорожденный ребенок имеет щелочной рН, равный 8-8,5. Щелочными являются такие жизненно важные среды организма как слюна человека, его слезы, женское грудное молоко и мужская семенная жидкость, панкреатический секрет. В отличие от желудочного сока с его высокой кислотностью, среда кишечника, особенно тонкого – преимущественно щелочная.
Поэтому сегодня особенно популярны теории Иосифа Локэмпер и Петера Ентшуры, итальянского доктора Симончини, который предлагает онкобольным проводить щелочную терапию, им вторит наш профессор Неумывакин, рекомендующий лечить целый ряд недугов пищевой содой – самой распространенным бытовым карбонатом.
И все же не стоит увлекаться экстремальными научными веяниями и опытам над собственным организмом. В организме, как и в любой природной системе, важна естественная гармония, которая, подчас, является очень тонкой и хрупкой. Доказательство – возьмем кислотно–щелочной баланс такой важной субстанции как кровь. Нормальный показатель рН человеческой крови 7,36-7,42. При самом незначительном сдвиге его в ту или иную сторону на 0,1 человек приобретает серьезную патологию, при сдвиге на 0,2 – впадает в кому, а при изменении всего лишь на 0,3 – умирает.
Нормальный показатель рН человеческой крови 7,36-7,42. При самом незначительном сдвиге его в ту или иную сторону на 0,1 человек приобретает серьезную патологию, при сдвиге на 0,2 – впадает в кому, а при изменении всего лишь на 0,3 – умирает.
Поэтому мы предлагаем поддерживать свой кислотно-щелочной баланс с помощью правильного питания. Ученые рекомендуют сформировать рацион так, чтобы на 80% он состоял из щелочных продуктов и лишь на 20% — из кислотных.
К щелочным относятся практически вся растительная пища, овощи и фрукты. Особенно (как ни странно!) лимоны; все виды огородной зелени; корнеплоды, такие как свёкла, редис, морковь; сельдерей; огурцы; чеснок; овощи крестоцветного вида и авокадо. Все это необходимо как можно чаще включать в свой рацион.
К сильно «закисляющим» наш организм продуктам относятся простые углевода – хлебо-булочные изделия из белой муки, разнообразная сдоба, макароны, шоколад и какао, пиво и сладкие безалкогольные напитки, а также говядина, свинина, моллюски, сыры. А из натурального растительного – грецкие орехи и арахис, черника, клюква, чернослив.
А из натурального растительного – грецкие орехи и арахис, черника, клюква, чернослив.
Важно помнить, что при нарушении гармонии веществ-антагонистов – кислот и щелочей – для нашего организма чревато дискомфортом и печальными последствиями. Однако пр разумном подходе каждый из нас может стать «хозяином» собственного кислотно-щелочного баланса! А значит – и здоровья, и активного долголетия.
Поделиться в соцсетях:
Кислоты, щелочи и шкала pH – сложные проценты
Нажмите, чтобы увеличитьШкала pH – это то, с чем мы все знакомы; большинство людей помнят его со школьных уроков химии. Это шкала, используемая для оценки того, насколько сильным является раствор кислоты (или щелочи). Цвета, связанные с каждым числом, соответствуют цвету универсального индикатора в растворах с этим конкретным pH. Изрядная часть людей, вероятно, не знает химии, лежащей в основе шкалы pH, но откуда именно берутся эти цифры?
Подсказки частично скрыты в названии весов.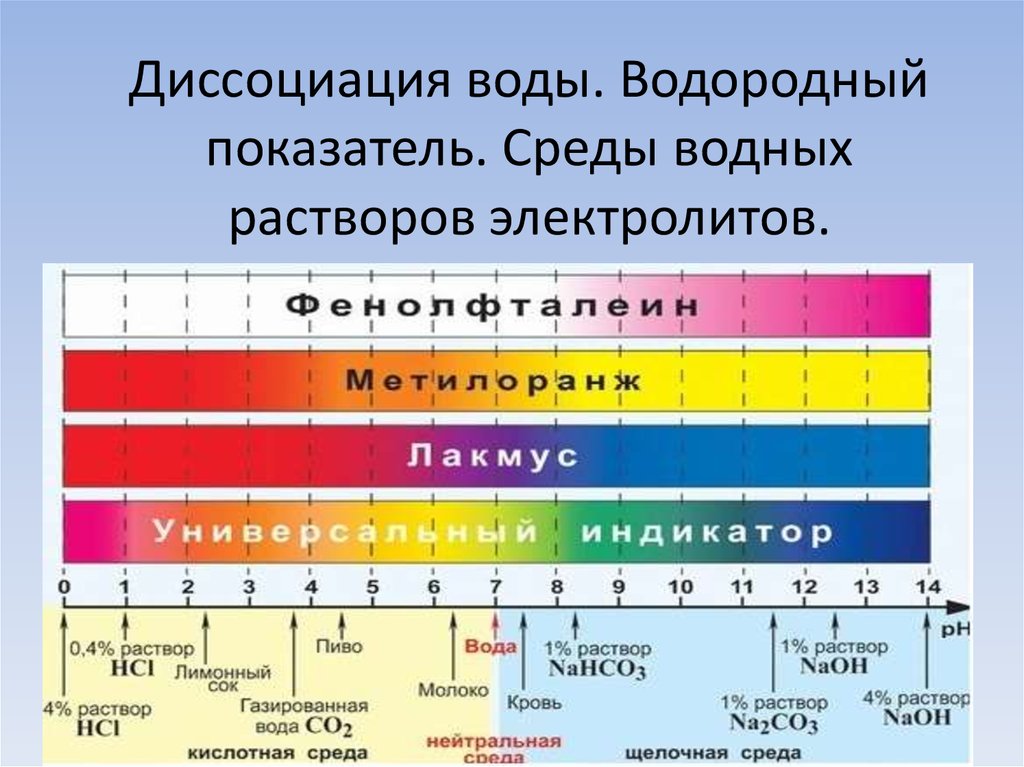
Глядя на график выше, вы можете видеть, что увеличение pH на одну точку фактически влечет за собой десятикратное уменьшение концентрации ионов водорода в растворе. Шкала — это так называемая логарифмическая шкала. Зачем нам вообще заниматься этой математической манипуляцией? Что ж, очевидно, что гораздо проще указать одну цифру, когда речь идет о кислотности (или щелочности) раствора, чем указать многозначную концентрацию ионов водорода.
Молекулы воды имеют химическую формулу H 2 O. Однако эти молекулы способны незначительно расщепляться в растворе на ионы H + и OH – (гидроксид). В нейтральном растворе концентрации этих двух ионов равны. Однако добавление кислоты или щелочи может привести к их изменению. Кислоты являются источником ионов водорода, и добавление их в воду увеличивает концентрацию ионов водорода в растворе, снижая концентрацию гидроксид-ионов. Для щелочей верно обратное: они уменьшают концентрацию ионов водорода, увеличивая при этом концентрацию ионов гидроксида.
Многие люди не понимают, что pH зависит от температуры. Строго говоря, чистая вода имеет pH 7 только при «комнатной температуре» (25°C). Выше и ниже этой температуры он может меняться: например, при 100°С рН чистой воды составляет 6,14, а при 0°С — 7,47. Это не означает, что чистая вода становится кислой или щелочной, но что при этих температурах именно эти значения pH представляют собой нейтральную точку. В качестве примечания также стоит отметить, что шкала pH не ограничивается обычным показанным здесь диапазоном от 0 до 14 — некоторые сильные кислоты и щелочи могут выходить за пределы этого диапазона, приводя к отрицательным значениям pH или значениям выше 14.
Это не означает, что чистая вода становится кислой или щелочной, но что при этих температурах именно эти значения pH представляют собой нейтральную точку. В качестве примечания также стоит отметить, что шкала pH не ограничивается обычным показанным здесь диапазоном от 0 до 14 — некоторые сильные кислоты и щелочи могут выходить за пределы этого диапазона, приводя к отрицательным значениям pH или значениям выше 14.
Еще одно распространенное заблуждение относительно pH касается человеческого тела. Такие диеты, как щелочная диета, утверждают, что можно повлиять на значение рН вашего тела, изменив свой рацион, включив в него «подщелачивающие» продукты, которые делают рН вашего тела более щелочным. Хотя то, что на самом деле предлагается, диета, богатая фруктами и овощами, безусловно, ни в коем случае не является вредной для здоровья, то, что вы едите, практически невозможно изменить pH вашего тела. Я не буду вдаваться в подробности, поскольку Кэт из блога The Chronicle Flask уже проделала отличную работу по развенчанию щелочных диет, но стоит повторить несколько ключевых моментов.
pH желудка может варьироваться от 1,5 до 3,5 по шкале pH. Однако это никак не влияет на pH нашего тела или, точнее, на нашу кровь. Человеческая кровь имеет значение рН, которое всегда слегка щелочное, между 7,35-7,45. Если бы мы могли целенаправленно изменять рН крови за пределами этого небольшого диапазона, мы могли бы на самом деле причинить себе немало вреда; даже изменение pH на 0,5 в любом случае может привести к необратимому повреждению клеток. К счастью, пища, которую мы едим, практически не влияет на рН крови.
То, что мы едим , может влиять на рН нашей мочи. pH мочи имеет среднее значение около 6, но может колебаться от 4,5 до 8. Однако, хотя вы можете иметь малейшее влияние на pH мочи с помощью диеты, это не связано с pH вашей крови; это остается в ранее указанном диапазоне, независимо от любого изменения рН мочи.
Идем дальше, и пока мы говорим о кислотах, стоит поговорить о силе кислот. Строго говоря, трудно разместить определенные химические соединения в определенных точках на шкале pH, поскольку их положение зависит от концентрации. Концентрация – это мера того, сколько вещества растворено в растворе. Если у нас есть много кислоты, растворенной в относительно небольшом количестве воды, мы бы сказали, что у нас есть раствор с высокой концентрацией. Точно так же, если бы у нас было очень мало кислоты, растворенной в большом количестве воды, у нас был бы раствор с низкой концентрацией.
Концентрация – это мера того, сколько вещества растворено в растворе. Если у нас есть много кислоты, растворенной в относительно небольшом количестве воды, мы бы сказали, что у нас есть раствор с высокой концентрацией. Точно так же, если бы у нас было очень мало кислоты, растворенной в большом количестве воды, у нас был бы раствор с низкой концентрацией.
Поскольку концентрацию растворов можно легко изменять, растворы одной и той же кислоты с различной концентрацией могут иметь разные значения pH. Однако некоторые кислоты сильнее других. Соляная кислота, та же кислота, что и желудочная кислота, является сильной кислотой, поскольку она может легко разделяться на составляющие ее ионы. С другой стороны, уксусная кислота, содержащаяся в уксусе, является сравнительно слабой кислотой — она не распадается на составляющие ее ионы. Другим примером слабой кислоты является фтористоводородная кислота; вопреки тому, во что вас уверяют в одном популярном телешоу на химическую тематику, на самом деле это довольно слабая кислота, которая, конечно же, не может растворить тело. Это неприятное соединение по разным причинам. Мы можем ранжировать кислоты с точки зрения их силы (или того, насколько легко они распадаются на составляющие их ионы), но это тема для другого поста!
Это неприятное соединение по разным причинам. Мы можем ранжировать кислоты с точки зрения их силы (или того, насколько легко они распадаются на составляющие их ионы), но это тема для другого поста!
Понравился этот пост и картинка? Рассмотрите возможность поддержки Compound Interest на Patreon и получайте превью предстоящих публикаций и многое другое!
Изображение в этой статье находится под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License. Ознакомьтесь с рекомендациями по использованию контента сайта.
Ссылки и дополнительная литература
- Удивительные щелочные лимоны – K Day, The Chronicle Flask
- Несколько замечаний по pH – M Leger, Atoms & Numbers
- Этот столб pH-сбалансирован для всех – M Leger, Atoms & Numbers
- pH, pOH и K a – Bodner Research Web
Нравится Загрузка…
Кислоты, основания и шкала pH
Эталонные материалы
Кислотные или основные?
Что такое кислота или основание?
Является ли жидкость кислотой или основанием, зависит от ионов водорода (обозначается химическим символом H + ). В воде (H 2 O) небольшое количество молекул диссоциирует (расщепляется). Некоторые молекулы воды теряют водород и превращаются в ионы гидроксида (ОН — ). «Потерянные» ионы водорода соединяются с молекулами воды, образуя ионы гидроксония (H 3 O + ). Для простоты ионы гидроксония обозначаются как ионы водорода H + . В чистой воде содержится равное количество ионов водорода и гидроксид-ионов. Раствор не является ни кислотным, ни щелочным.
В воде (H 2 O) небольшое количество молекул диссоциирует (расщепляется). Некоторые молекулы воды теряют водород и превращаются в ионы гидроксида (ОН — ). «Потерянные» ионы водорода соединяются с молекулами воды, образуя ионы гидроксония (H 3 O + ). Для простоты ионы гидроксония обозначаются как ионы водорода H + . В чистой воде содержится равное количество ионов водорода и гидроксид-ионов. Раствор не является ни кислотным, ни щелочным.
Кислота представляет собой вещество, отдающее ионы водорода. Из-за этого при растворении кислоты в воде баланс между ионами водорода и гидроксид-ионами смещается. Теперь в растворе больше ионов водорода, чем ионов гидроксида. Такой раствор кислый.
Основание — это вещество, которое принимает ионы водорода. При растворении основания в воде баланс между ионами водорода и гидроксид-ионами смещается в противоположную сторону. Поскольку основание «впитывает» ионы водорода, в результате получается раствор с большим количеством ионов гидроксида, чем ионов водорода. Такой раствор является щелочным.
Такой раствор является щелочным.
Что такое рН?
Кислотность и щелочность измеряются по логарифмической шкале, называемой pH . Вот почему: в сильнокислом растворе может быть в сто миллионов миллионов или в сто триллионов (100 000 000 000 000) раз больше ионов водорода, чем в сильно щелочном растворе! Обратной стороной, конечно же, является то, что сильно щелочной раствор может содержать в 100 000 000 000 000 раз больше гидроксид-ионов, чем сильнокислый раствор. Более того, концентрации ионов водорода и гидроксид-ионов в повседневных растворах могут варьироваться во всем этом диапазоне.
Чтобы легче было работать с этими большими числами, ученые используют логарифмическую шкалу , шкалу рН. Каждая единица изменения шкалы pH соответствует десятикратному изменению концентрации ионов водорода. Теоретически шкала pH является открытой, но большинство значений pH находится в диапазоне от 0 до 14. Гораздо проще использовать логарифмическую шкалу вместо того, чтобы постоянно записывать все эти нули! Кстати, обратите внимание, что сто миллионов миллионов — это единица с четырнадцатью нулями после нее? Это не совпадения, это логарифмы!
Чтобы быть более точным, pH представляет собой отрицательный логарифм концентрации ионов водорода:
pH = -log [H + ]
Квадратные скобки вокруг H + автоматически означают «концентрация» для химика. Это уравнение означает именно то, о чем мы говорили ранее: при изменении рН на 1 единицу концентрация ионов водорода изменяется в десять раз. Чистая вода имеет нейтральный рН 7. Значения рН ниже 7 являются кислыми, а значения рН выше 7 являются щелочными (основными). В таблице 1 приведены примеры веществ с различными значениями pH (Decelles, 2002; Environment Canada, 2002; EPA, дата неизвестна).
Это уравнение означает именно то, о чем мы говорили ранее: при изменении рН на 1 единицу концентрация ионов водорода изменяется в десять раз. Чистая вода имеет нейтральный рН 7. Значения рН ниже 7 являются кислыми, а значения рН выше 7 являются щелочными (основными). В таблице 1 приведены примеры веществ с различными значениями pH (Decelles, 2002; Environment Canada, 2002; EPA, дата неизвестна).
Общие примеры кислот и оснований
Измерение pH
Как вы измеряете pH?
pH жидкости или раствора часто является важной частью научной информации. Измерить рН можно просто и быстро, используя индикаторную бумагу , индикаторную палочку или рН-метр . Бумага для измерения рН и индикаторные палочки представляют собой кусочки бумаги или более жесткие палочки, содержащие индикаторов рН (химические вещества, которые меняют цвет в зависимости от того, насколько кислым или щелочным является раствор). Для измерения рН в жидкость погружают кусочек индикаторной бумаги или индикаторную палочку. Затем цвет смоченной бумаги/палочки сопоставляется с цветовым кодом, который поставляется с контейнером с индикаторной бумагой или индикаторными палочками. Каждый цвет на клавише соответствует своему уровню pH. Пример использованной палочки-индикатора pH и соответствующей цветовой маркировки показан ниже на рисунке 1. pH-метры — это электронные устройства, используемые для измерения pH. Они состоят из зонда, погруженного в раствор, и цифрового считывающего устройства. pH-метры даже более точны, чем pH-метры или индикаторные палочки. В приведенной ниже Таблице 2 обсуждается, какие типы устройств для измерения pH лучше всего подходят для различных научных проектов, а также предлагается быстрая ссылка для приобретения различных индикаторных полосок и индикаторной бумаги для измерения pH.
Затем цвет смоченной бумаги/палочки сопоставляется с цветовым кодом, который поставляется с контейнером с индикаторной бумагой или индикаторными палочками. Каждый цвет на клавише соответствует своему уровню pH. Пример использованной палочки-индикатора pH и соответствующей цветовой маркировки показан ниже на рисунке 1. pH-метры — это электронные устройства, используемые для измерения pH. Они состоят из зонда, погруженного в раствор, и цифрового считывающего устройства. pH-метры даже более точны, чем pH-метры или индикаторные палочки. В приведенной ниже Таблице 2 обсуждается, какие типы устройств для измерения pH лучше всего подходят для различных научных проектов, а также предлагается быстрая ссылка для приобретения различных индикаторных полосок и индикаторной бумаги для измерения pH.
Чтобы получить точные показания pH, всегда помните:
- Подождите минуту или две после добавления в раствор кислоты или основания. Это позволит завершить реакцию (отдаваемые ионы [кислота] или принимаемые [основание]) до того, как вы измерите.

- Хорошо взболтайте или перемешайте раствор перед измерением. Это поможет обеспечить однородность раствора.
При использовании индикаторной бумаги/индикаторных палочек pH необходимо также:
- Используйте только бумагу/палочки, которые не были предварительно смочены.
- Подождите, пока цвет перестанет меняться (максимум 1–2 минуты), прежде чем сопоставлять бумагу/карандаш с цветовым ключом. Не ждите более 5 минут после стабилизации цвета, иначе он может начать тускнеть, что повлияет на точность показаний.
При использовании рН-метра вы также должны:
- Внимательно прочесть руководство к рН-метру перед его использованием.
- Промывайте датчик рН-метра дистиллированной водой перед каждым измерением.
- Используйте растворы с известными значениями pH, см. Таблицу 2, чтобы убедиться, что pH-метр точно откалиброван.
- Прежде чем снимать показания, убедитесь, что датчик рН-метра полностью погружен в раствор.


