Салициловая кислота свойства: применение в косметике и свойства
Салициловая кислота (cалицилаты, салициламид)
Салициловая кислота – одно из наиболее известных и широко применяемых обезболивающих, жаропонижающих и противовоспалительных средств. Сама салициловая кислота используется местно в связи с ее кератолитическими, бактериостатическими, фунгицидными и фотозащитными свойствами. Производные салициловой кислоты также применяются в медицине как жаропонижающие, противоревматические, противовоспалительные и обезболивающие средства.
Синонимы русские
Аспирин, неацитилированные салицилаты.
Синонимы английские
Salicylic acid, Salicylamide, Salicylamidum.
Метод исследования
Высокоэффективная жидкостная хроматография с тандемной масс-спектрометрией.
Единицы измерения
мкг/мл (микрограмм на миллилитр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?

- Не принимать пищу в течение 2-3 часов до исследования, можно пить чистую негазированную воду.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Салициловая кислота – 2-гидроксибензойная, или фенольная, кислота, получившая свое название в честь ивы (от лат. salix «ива»), из коры которой она впервые была выделена. Салициловая кислота и салицилаты, а также её сложные эфиры и другие синтетические производные салициловой кислоты обладают выраженным противовоспалительным действием. Салициловая кислота обладает слабыми антисептическими, раздражающими и кератолитическими свойствами и применяется наружно в мазях и растворах при лечении кожных заболеваний. В ряде исследований было показано, что местное применение салициловой кислоты снижает скорость пролиферации кератиноцитов, ингибирует холестеринсульфотрансферазу, фермент, ответственный за образование сульфата холестерина в кератиноцитах.
Выделяют ацетилированные и неацитилированные салицилаты – производные салициловой кислоты. К ацетилированным салицилатам относится ацетилсалициловая кислота (аспирин). Ее назначают как противовоспалительное, жаропонижающее и болеутоляющее средство. Кроме того, аспирин применяют для подавления агрегации тромбоцитов и профилактики тромбозов. Механизм антиагрегационного действия ацетилсалициловой кислоты связан с нарушением синтеза тромбоксана A2.
К ацетилированным салицилатам относится ацетилсалициловая кислота (аспирин). Ее назначают как противовоспалительное, жаропонижающее и болеутоляющее средство. Кроме того, аспирин применяют для подавления агрегации тромбоцитов и профилактики тромбозов. Механизм антиагрегационного действия ацетилсалициловой кислоты связан с нарушением синтеза тромбоксана A2.
Неацетилированные салицилаты (натрия салицилат, салициламид) имеют меньшую антипростагландиновую активность, поэтому осложнения, связанные с блокадой простагландинов, встречаются реже. Эти препараты практически не влияют на функцию тромбоцитов и реже вызывают геморрагические осложнения. Неацетилированные салицилаты применяют в качестве противовоспалительного средства. Салициламид блокирует циклооксигеназу, нарушает метаболизм арахидоновой кислоты, уменьшает количество простагландинов как в очаге воспаления, так и в здоровых тканях, подавляет экссудативную и пролиферативную фазу воспаления. Обезболивающее действие салициламида обусловлено снижением концентрации биогенных аминов, обладающих альгогенными свойствами, и увеличением порога болевой чувствительности рецепторного аппарата.
Для чего используется исследование?
- Для определения концентрации препарата в крови.
- Для подбора индивидуальной дозировки препарата.
- Для оптимизации контроля за лечением с помощью коррекции дозы.
- Для оценки лекарственного взаимодействия.
- Для диагностики передозировки.
- Для выявления нарушений по режиму приема препарата.
- Для предотвращения токсического действия препарата.
Когда назначается исследование?
- При назначении препарата для лечения.
- При необходимости определения концентрации препарата и мониторинга ее колебаний в крови.
- При недостаточной эффективности применяемого препарата и решении вопроса о коррекции дозы.

- При изменении дозировки и лекарственной формы препарата.
- При подозрении на передозировку препаратом.
Что означают результаты?
Референсные значения: 5 — 300 мкг/мл.
Результаты исследования оцениваются лечащим врачом с учетом дозы салициловой кислоты, режима приема, возраста пациента, сопутствующей патологии и индивидуальной переносимости препарата.
Что может влиять на результат?
- Концентрация салициловой кислоты в сыворотке крови может меняться у пациентов с почечной, печеночной недостаточностью.
- Антациды, препараты магния, алюминия могут уменьшать концентрацию салициловой кислоты в крови из-за замедления и снижения ее всасывания.
- Концентрация ацетилсалициловой кислоты может повышаться при одновременном приеме кофеина, этанола, метопролола, дипиридамола.
Важные замечания
- Во время лечения препаратами салициловой кислоты необходимо контролировать клинический анализ крови и биохимический анализ крови (печеночные ферменты).

- Во время продолжительной терапии препаратами ацетилсалициловой кислоты следует проводить исследование кала на скрытую кровь.
Кто назначает исследование?
Терапевт, кардиолог, дерматолог, инфекционист, врач общей практики, ревматолог, невролог, стоматолог, травматолог, хирург.
Литература
- Madan, R. K., & Levitt, J. (2014). A review of toxicity from topical salicylic acid preparations. Journal of the American Academy of Dermatology, 70(4), 788 – 792. doi:10.1016/j.jaad.2013.12.005.
- https://www.rlsnet.ru/books_book_id_4_page_52.htm.
область применения и причины противопоказаний для использования гидроксибензойной кислоты — комментарии от ПраймКемикалсГрупп
Салициловая кислота принадлежит к классу ароматических кислот. Она отличается от бензойной наличием гидроксильной группы при атоме углерода в орто-положении. Еще ее называют 2-гидроксибензойной или фенольной.
История и современные способы получения
Вещество было впервые получено из природного сырья – ивовой коры и эфирного масла некоторых сортов спиреи. В настоящее время ее производят в ходе реакции Кольбе – Шмитта. При повышенной температуре и давлении на натриевую соль бензойной кислоты воздействуют углекислым газом. Продукт реакции на следующем этапе обрабатывают соляной кислотой.
Более современным методом является способ Марассе – при гораздо более жестких условиях углекислый газ продувают через смесь фенола и карбоната калия.
Свойства и основанные на них способы применения
2-гидроксибензойная кислота – отличный антисептик. Раньше она широко использовалась в качестве пищевого консерванта. Однако имеется ряд моментов, серьезно ограничивающих применение салициловой кислоты в этом качестве:
• во-первых, при нагревании она выделяет фенол. Это вещество портит вкус и запах продуктов и является ядом;
• во-вторых, при контакте с металлами реагент может вызвать неэстетичное изменение цвета продукта.
В медицине антисептические свойства данного вещества используются более широко и успешно. Многие знают, что такое «болтушка» салициловая. Применение ее в качестве наружного средства позволяет избавиться от юношеских прыщей, стимулирует активное отслаивание клеток кожи и их обновление. Она также входит в состав средств от перхоти и себорейного дерматита, помогает избавиться от бородавок и натоптышей, размягчая ороговевшую кожу и способствуя ее удалению.
При приеме внутрь вещество действует как жаропонижающее, хотя более успешно с этим справляется производная от него кислота – ацетилсалициловая. Она используется также в качестве сырья для производства некоторых красителей и душистых веществ. В основном, такими свойствами обладают ее сложные эфиры.
В аналитической химии реагент используется для колориметрического определения ионов некоторых металлов, например, железа и меди, а также для выделения тория из смесей с другими элементами.
В каких случаях нельзя использовать салициловую кислоту и почему
При наружном применении нельзя наносить препараты, содержащие этот компонент, на поврежденную или очень сухую кожу. Прием внутрь в качестве жаропонижающего запрещен для беременных женщин и детей в возрасте до 12 лет. Это связано с риском возникновения синдрома Рея – серьезного токсического повреждения печени и головного мозга.
Прием внутрь в качестве жаропонижающего запрещен для беременных женщин и детей в возрасте до 12 лет. Это связано с риском возникновения синдрома Рея – серьезного токсического повреждения печени и головного мозга.
Как приобрести реагент в ПраймКемикалсГрупп
В ассортименте «ПраймКемикалсГрупп» имеется салициловая кислота в упаковке по 1000 г. Вы можете заказать любое количество этого реагента, связавшись с оператором магазина, либо самостоятельно, с помощью кнопки «Купить», расположенной на соответствующей странице каталога.
САЛИЦИЛОВАЯ КИСЛОТА | CAMEO Chemicals
Добавить в MyChemicals Страница для печати
Химический паспорт
Химические идентификаторы
Что это за информация?
Поля химического идентификатора
включают общие идентификационные номера,
алмаз NFPA
Знаки опасности Министерства транспорта США и общий
описание хим. Информация в CAMEO Chemicals поступает
из множества
источники данных.
Информация в CAMEO Chemicals поступает
из множества
источники данных.
| Номер CAS | Знак опасности DOT | Береговая охрана США КРИС Код | |
|---|---|---|---|
| никто | данные недоступны |
|
| Карманный справочник NIOSH | Международная карта химической безопасности | ||
| никто |
| ||
NFPA 704
| Алмаз | Опасность | Значение | Описание |
|---|---|---|---|
| Здоровье | 1 | Может вызвать сильное раздражение.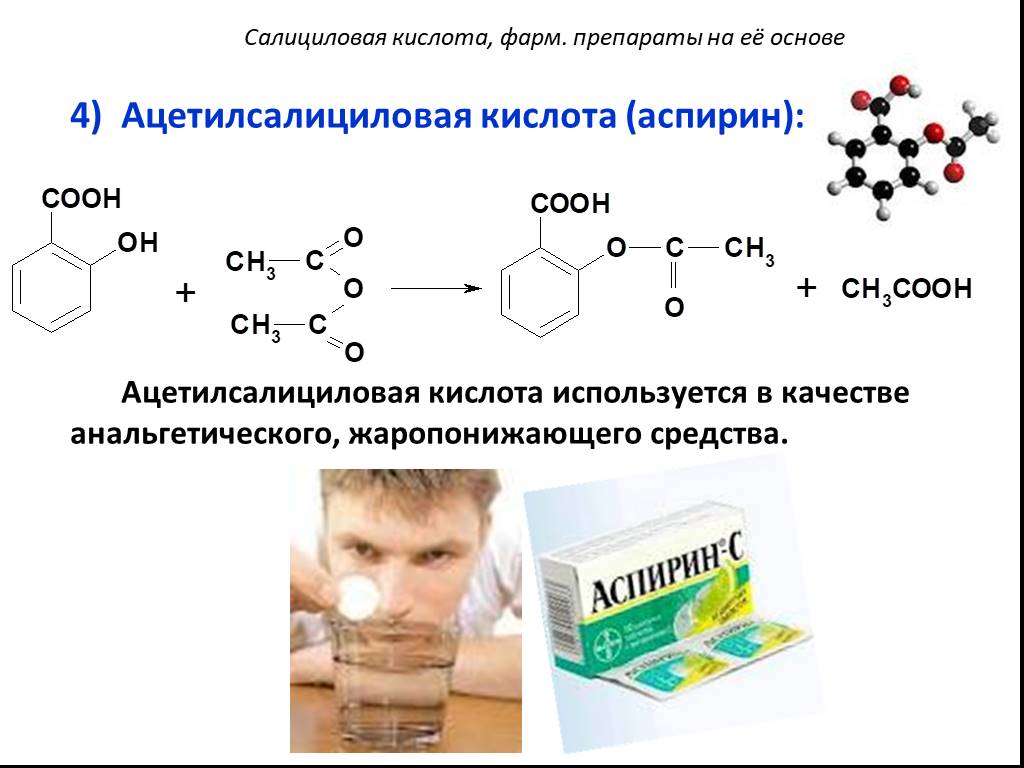 | |
| Воспламеняемость | Должен быть предварительно нагрет до воспламенения. | ||
| нестабильность | 0 | Обычно стабилен даже в условиях пожара. | |
| Особенный |
(NFPA, 2010)
Общее описание
Твердое вещество от белого до светло-коричневого цвета без запаха. Тонет и медленно смешивается с водой. (USCG, 1999)
Опасности
Что это за информация?
Опасные поля
включать
специальные предупреждения об опасности
воздух и вода
реакции, пожароопасность, опасность для здоровья, профиль реактивности и
подробности о
задания реактивных групп
и
потенциально несовместимые абсорбенты.
Информация в CAMEO Chemicals поступает из различных источников.
Предупреждения о реактивности
нет
Реакции с воздухом и водой
Возгоняется и образует пары или пыль, которые могут взорваться (USCG, 1999).
Пожароопасность
Особая опасность продуктов горения: При пожаре могут образовываться раздражающие пары несгоревшего материала и фенола.
Поведение в огне: возгоняется и образует пары или пыль, которые могут взорваться (USCG, 1999)
Опасность для здоровья
Вдыхание пыли вызывает раздражение носа и горла. Рвота может возникнуть спонтанно при проглатывании больших количеств. Контакт с глазами вызывает раздражение, выраженную боль и повреждение роговицы, которое должно зажить. Длительный или повторяющийся контакт с кожей может вызвать заметное раздражение или даже легкий ожог. (USCG, 1999)
Профиль реактивности
САЛИЦИЛОВАЯ КИСЛОТА представляет собой карбоновую кислоту. Карбоновые кислоты отдают ионы водорода, если присутствует основание, способное их принять. Так они реагируют со всеми основаниями, как органическими (например, амины), так и неорганическими. Их реакции с основаниями, называемые «нейтрализациями», сопровождаются выделением значительного количества тепла. Нейтрализация между кислотой и основанием дает воду плюс соль. Карбоновые кислоты с шестью и менее атомами углерода хорошо или умеренно растворимы в воде; те, у которых больше шести атомов углерода, мало растворимы в воде. Растворимая карбоновая кислота в некоторой степени диссоциирует в воде с образованием ионов водорода. Поэтому рН растворов карбоновых кислот меньше 7,0. Многие нерастворимые карбоновые кислоты быстро реагируют с водными растворами, содержащими химическое основание, и растворяются по мере того, как при нейтрализации образуется растворимая соль. Карбоновые кислоты в водном растворе и жидкие или расплавленные карбоновые кислоты могут реагировать с активными металлами с образованием газообразного водорода и соли металла. Такие реакции в принципе происходят и для твердых карбоновых кислот, но они медленны, если твердая кислота остается сухой.
Так они реагируют со всеми основаниями, как органическими (например, амины), так и неорганическими. Их реакции с основаниями, называемые «нейтрализациями», сопровождаются выделением значительного количества тепла. Нейтрализация между кислотой и основанием дает воду плюс соль. Карбоновые кислоты с шестью и менее атомами углерода хорошо или умеренно растворимы в воде; те, у которых больше шести атомов углерода, мало растворимы в воде. Растворимая карбоновая кислота в некоторой степени диссоциирует в воде с образованием ионов водорода. Поэтому рН растворов карбоновых кислот меньше 7,0. Многие нерастворимые карбоновые кислоты быстро реагируют с водными растворами, содержащими химическое основание, и растворяются по мере того, как при нейтрализации образуется растворимая соль. Карбоновые кислоты в водном растворе и жидкие или расплавленные карбоновые кислоты могут реагировать с активными металлами с образованием газообразного водорода и соли металла. Такие реакции в принципе происходят и для твердых карбоновых кислот, но они медленны, если твердая кислота остается сухой. Даже «нерастворимые» карбоновые кислоты могут поглощать из воздуха достаточно воды и достаточно растворяться в ней, чтобы вызвать коррозию или растворение железных, стальных и алюминиевых деталей и контейнеров. Карбоновые кислоты, как и другие кислоты, реагируют с солями цианидов с образованием газообразного цианистого водорода. Реакция протекает медленнее для сухих твердых карбоновых кислот. Нерастворимые карбоновые кислоты реагируют с растворами цианидов с выделением газообразного цианистого водорода. Горючие и/или токсичные газы и тепло образуются при реакции карбоновых кислот с диазосоединениями, дитиокарбаматами, изоцианатами, меркаптанами, нитридами и сульфидами. Карбоновые кислоты, особенно в водном растворе, также реагируют с сульфитами, нитритами, тиосульфатами (с образованием H3S и SO3), дитионитами (SO2) с образованием горючих и/или токсичных газов и тепла. Их реакция с карбонатами и бикарбонатами приводит к образованию безвредного газа (углекислого газа), но все же тепла. Как и другие органические соединения, карбоновые кислоты могут окисляться сильными окислителями и восстанавливаться сильными восстановителями.
Даже «нерастворимые» карбоновые кислоты могут поглощать из воздуха достаточно воды и достаточно растворяться в ней, чтобы вызвать коррозию или растворение железных, стальных и алюминиевых деталей и контейнеров. Карбоновые кислоты, как и другие кислоты, реагируют с солями цианидов с образованием газообразного цианистого водорода. Реакция протекает медленнее для сухих твердых карбоновых кислот. Нерастворимые карбоновые кислоты реагируют с растворами цианидов с выделением газообразного цианистого водорода. Горючие и/или токсичные газы и тепло образуются при реакции карбоновых кислот с диазосоединениями, дитиокарбаматами, изоцианатами, меркаптанами, нитридами и сульфидами. Карбоновые кислоты, особенно в водном растворе, также реагируют с сульфитами, нитритами, тиосульфатами (с образованием H3S и SO3), дитионитами (SO2) с образованием горючих и/или токсичных газов и тепла. Их реакция с карбонатами и бикарбонатами приводит к образованию безвредного газа (углекислого газа), но все же тепла. Как и другие органические соединения, карбоновые кислоты могут окисляться сильными окислителями и восстанавливаться сильными восстановителями. Эти реакции выделяют тепло. Возможен широкий ассортимент продукции. Как и другие кислоты, карбоновые кислоты могут инициировать реакции полимеризации; как и другие кислоты, они часто катализируют (увеличивают скорость) химических реакций.
Эти реакции выделяют тепло. Возможен широкий ассортимент продукции. Как и другие кислоты, карбоновые кислоты могут инициировать реакции полимеризации; как и другие кислоты, они часто катализируют (увеличивают скорость) химических реакций.
Принадлежит к следующей реакционной группе(ам):
- Кислоты карбоновые
- Фенолы и крезолы
Потенциально несовместимые абсорбенты
Информация отсутствует.
Рекомендации по реагированию
Что это за информация?
Поля рекомендации ответа включают в себя расстояния изоляции и эвакуации, а также рекомендации по пожаротушение, пожарное реагирование, защитная одежда и первая помощь. информация в CAMEO Chemicals поступает из различных источники данных.
Изоляция и эвакуация
Информация отсутствует.
Пожаротушение
Неиспользуемые средства пожаротушения: вода или пена могут вызвать пенообразование.
Средства пожаротушения: вода, пена, сухой химикат, двуокись углерода (USCG, 1999)
Non-Fire Response
Информация отсутствует.
Защитная одежда
Перчатки; очки для плавания; респиратор от пыли; чистая одежда, закрывающая тело (USCG, 1999)
DuPont Tychem® Suit Fabrics
Информация отсутствует.
Первая помощь
Вдыхание: выйти на свежий воздух.
ПРОГЛАТЫВАНИЕ: вызвать рвоту и немедленно обратиться к врачу.
ГЛАЗА: немедленно промыть водой в течение 15 мин. и получить медицинскую помощь.
КОЖА: промыть водой с мылом. (Геологическая служба США, 1999 г.)
Физические свойства
Что это за информация?
Поля физических свойств
включают в себя такие свойства, как давление пара и
температура кипения, а также пределы взрываемости и
пороги токсического воздействия
Информация в CAMEO Chemicals поступает из различных источников. источники данных.
источники данных.
| Химическая формула: |
|
Температура вспышки: данные отсутствуют
Нижний предел взрываемости (НПВ): данные отсутствуют
Верхний предел взрываемости (ВПВ): данные отсутствуют
Температура самовоспламенения: данные отсутствуют
Температура плавления: 315°F (USCG, 1999)
Давление пара: данные отсутствуют
Плотность пара (относительно воздуха): данные отсутствуют
Удельный вес: 1,44 при 68°F (USCG, 1999)
Температура кипения: данные недоступны
Молекулярная масса: 138,13 (USCG, 1999)
Растворимость в воде: данные отсутствуют
Энергия/потенциал ионизации: данные отсутствуют
IDLH: данные отсутствуют
AEGL (рекомендательные уровни острого воздействия)
Информация об AEGL отсутствует.ERPG (Руководство по планированию реагирования на чрезвычайные ситуации)
Информация о ERPG отсутствует.
PAC (критерии защитных действий)
Информация о PAC отсутствует.Нормативная информация
Что это за информация?
Поля нормативной информации включить информацию из Сводный список III Агентства по охране окружающей среды США списки, Химический завод Агентства кибербезопасности и безопасности инфраструктуры США антитеррористические стандарты, и Управление по охране труда и здоровья США Перечень стандартов по управлению безопасностью технологического процесса при работе с особо опасными химическими веществами (подробнее об этих источники данных).
Сводный перечень списков EPA
Отсутствует нормативная информация.
Антитеррористические стандарты CISA Chemical Facility (CFATS)
Отсутствует нормативная информация.
Список стандартов OSHA по управлению безопасностью процессов (PSM)
Отсутствует нормативная информация.
Альтернативные химические названия
Что это за информация?
В этом разделе приводится список альтернативных названий этого химического вещества, включая торговые названия и синонимы.
- КИСЛОТА О-ГИДРОКСИБЕНЗОЙНАЯ
- ЗАМЕДЛИТЕЛЬ W
- КИСЛОТА САЛИЦИЛОВАЯ
Значение, структура, свойства, эффекты, применение
Органическое вещество салициловая кислота имеет молекулярную формулу \(\mathrm{C}_{7} \mathrm{H}_{6} \mathrm{O}_{3 }\). Это подтип бета-гидроксикислоты (BHA) и фенольной кислоты. Салициловая кислота всегда была моногидроксибензойной кислотой, то есть бензойной кислотой с орто-гидроксигруппой. Салициловая кислота, также известная как 2-гидроксибензойная кислота, впервые была выделена из листьев ивы рода Salix.
Служит гормоном для растений. Такая липофильная моногидроксибензойная кислота получается при метаболизме салицина.
В этой статье мы узнаем о салициловой кислоте, ее структуре, формуле, физических и химических свойствах, способе приготовления, побочных эффектах и применении.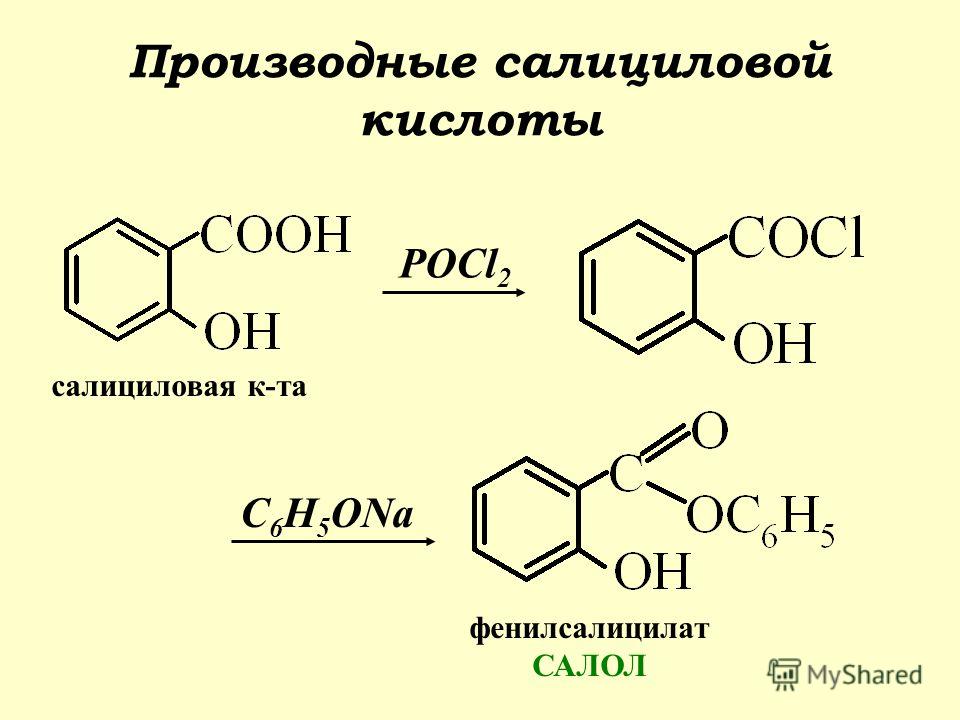
Салициловая кислота
Бетагидроксикислота, т. е. салициловая кислота, является важным природным растительным веществом. Помимо действия в качестве терапевтического антибактериального средства, он обладает значительным противовоспалительным эффектом. Салициловая кислота представляет собой вещество от бесцветного до светло-коричневого цвета без запаха, медленно тонет и соединяется с водой.
Это органическая карбоновая кислота, которая является кристаллической и обладает кератолитическим, бактерицидным и фунгицидным действием. Однако при приеме внутрь в чрезмерных количествах он токсичен. Следовательно, его можно рассматривать как антисептик и пищевой консервант при употреблении в умеренных количествах. Он состоит из \(\mathrm{COOH}\) карбоксильной группы. Он не имеет цвета и запаха и является важнейшим ингредиентом в производстве нескольких лекарственных препаратов, в том числе аспирина.
Салициловая кислота представляет собой моногидроксибензойную кислоту, представляющую собой бензойную кислоту с орто-гидроксигруппой. Его делают из листьев грушанки и коры белой ивы. Он действует как метаболит растений, метаболит водорослей, антимикробный реагент, антибактериальный агент, кератолитическое лекарство и растительный гормон. Это сопряженная кислота салицилата (сопряженная кислота образуется при присоединении протона к основанию) 9{2}\) гибридизовал все свои атомы углерода. В результате внутри самой салициловой кислоты возникает водородная связь.
Его делают из листьев грушанки и коры белой ивы. Он действует как метаболит растений, метаболит водорослей, антимикробный реагент, антибактериальный агент, кератолитическое лекарство и растительный гормон. Это сопряженная кислота салицилата (сопряженная кислота образуется при присоединении протона к основанию) 9{2}\) гибридизовал все свои атомы углерода. В результате внутри самой салициловой кислоты возникает водородная связь.
Салициловая кислота разлагается с высвобождением протона из карбоновой кислоты в водном растворе. Наблюдается внутримолекулярная водородная связь. Гидроксильная группа (ОН) имеет внутримолекулярную водородную связь с карбоновой кислотой (\(\mathrm{COOH}\)), как показано на рисунке выше.
Подготовка
Салициловая кислота производится из различных исходных продуктов, таких как фенолы, метилсалицилат и т.д., по механизму реакции для промышленного получения.
Из фенолов
Феноксид натрия получают всякий раз, когда фенол реагирует с гидроксидом натрия, который затем подвергают дистилляции и дегидратации.
Салицилат натрия образуется в результате процесса карбоксилирования, происходящего после реакции с диоксидом углерода (соль салициловой кислоты). Солевая форма соединяется с разбавленной кислотой (ион гидроксония или любой другой вид, который обозначает протон) для создания салициловой кислоты.
Реакция Кольбе-Шмитта
Салициловая кислота, предшественник аспирина, производится с помощью важной для промышленности реакции Кольбе-Шмитта. Эта реакция известна как реакция Кольбе-Шмитта . Ион натрия должен координироваться с двумя атомами кислорода — одним из феноксида и одним из \(\mathrm{CO}_{2}\) — поскольку орто-производное показывает эффективную доставку электрофила, орто-положение достигается.
Механизм реакции Кольбе-Шмитта
Реакция Кольбе-Шмитта протекает следующим образом:
Первым этапом реакции Кольбе-Шмитта является депротонирование фенола ионами гидроксида. Далее следует произвести феноксид (сопряженное основание фенола).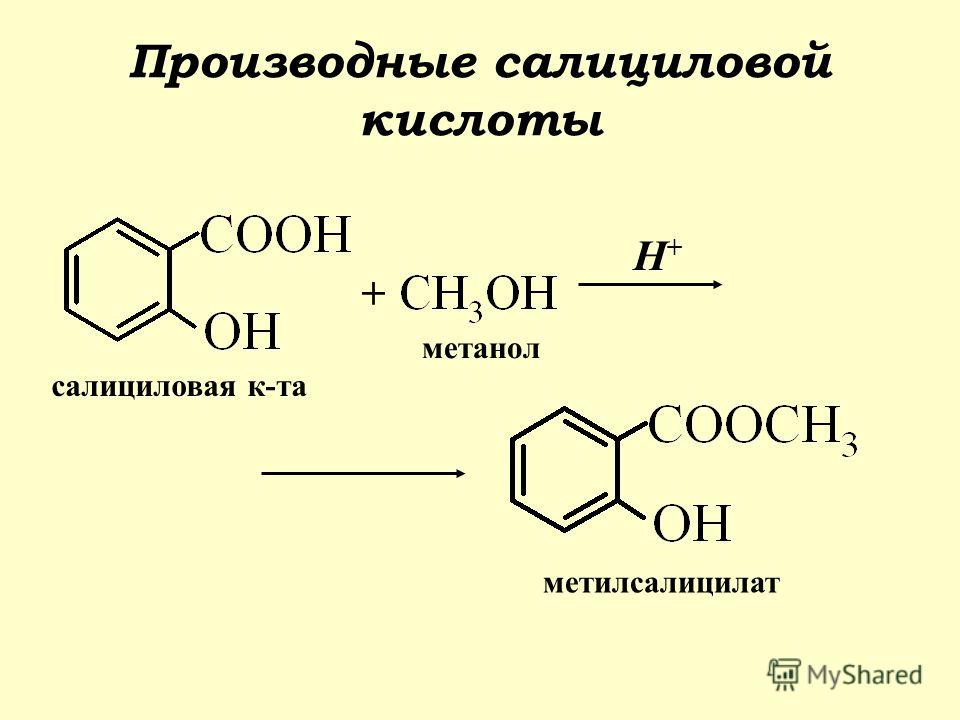 Карбоксилат образуется, когда феноксид, алкоксид и енолятный нуклеофил реагируют с диоксидом углерода. Затем сильная кислота, такая как водная серная кислота, протонирует карбоксилат. Таутомеризация, катализируемая кислотой, затем восстанавливает ароматичность.
Карбоксилат образуется, когда феноксид, алкоксид и енолятный нуклеофил реагируют с диоксидом углерода. Затем сильная кислота, такая как водная серная кислота, протонирует карбоксилат. Таутомеризация, катализируемая кислотой, затем восстанавливает ароматичность.
Реакция Реймера-Тимана
Самый простой метод реакции Реймера-Тимана, который используется для ортоформилирования фенолов, заключается в превращении фенола в салициловый альдегид. Карл Реймер и Фердинанд Тиманн были теми, кто обнаружил ответ.
Механизм реакции Реймера-Тиманна
Реакция Реймера-Тиманна протекает следующим образом: производят дихлоркарбен (3), основные реакционноспособные частицы. Кроме того, фенол (4) будет депротонирован гидроксидом с образованием отрицательно заряженного феноксида (5). Ароматическое кольцо становится значительно более нуклеофильным, поскольку в нем делокализован отрицательный заряд. Промежуточный дихлорметилзамещенный фенол образуется при атаке дихлоркарбена нуклеофилом (7). Требуемый товар (9) создается после основного гидролиза.
Требуемый товар (9) создается после основного гидролиза.
Из салицилового альдегида
\(KMnO_4\) можно использовать для получения салициловой кислоты из салицилового альдегида без окисления гидроксильной группы (ОН).
Поскольку атом C, присоединенный к гидроксильной группе, уже использовал два электрона для сигма-связи и один электрон для пи-связи, гидроксильная группа, присоединенная к бензолу, не окислялась.
Из метилсалицилата путем радикального образования
Фармацевтический сектор также хорошо известен использованием болеутоляющего метилсалицилата (масло грушанки). Его можно использовать для создания салициловой кислоты. В этом процессе метилсалицилат соединяется с гидроксидом натрия с образованием динатриевого салицилата. Это промежуточная натриевая соль салициловой кислоты. Затем это промежуточное соединение смешивают с серной кислотой для получения салициловой кислоты.
Гидроксильная группа метилсалицилата взаимодействует с гидроксид-ионом с образованием феноксидного радикала. При дальнейшей реакции он выбрасывает метоксигруппу \((\mathrm{OCH}_3)\), которая образует в побочном продукте метанол, тем самым образуя салициловую кислоту в качестве основного продукта.
При дальнейшей реакции он выбрасывает метоксигруппу \((\mathrm{OCH}_3)\), которая образует в побочном продукте метанол, тем самым образуя салициловую кислоту в качестве основного продукта.
Из метилсалицилата путем омыления
Омыление представляет собой необратимый щелочной гидролиз сложных эфиров. Здесь два моля гидроксида натрия и один моль метанола и воды реагируют с образованием салицилата натрия из одного моля метилсалицилата (масло грушанки). Салицилат натрия обрабатывают серной или соляной кислотой для удаления иона натрия. В результате в качестве побочных продуктов образуются салициловая кислота и сульфат натрия.
Свойства салициловой кислоты
Салициловая кислота имеет различные свойства и может быть описана следующим образом:
Физические свойства
- Химическая формула салициловой кислоты \(\mathrm{C}_{7} \mathrm{H }_{6} \mathrm{O}_{3}\)
- Его название IUPAC записывается как 2-гидроксибензойная кислота.
- Молекулярная масса 138,12 г/моль
- Кристаллы игольчатой формы, бесцветные или белого цвета с едким вкусом и без запаха.

- Другими синонимами являются салициловая кислота, о-гидроксибензойная кислота, 2-карбоксифенол.
- Плотность 1,44 при 20 ⁰C, температура плавления 315 ⁰C, температура кипения 211 ⁰C при pH 2,4.
- Из-за своей липофильной природы очень плохо растворяется в воде.
- Салициловая кислота растворима в органических растворителях, таких как четыреххлористый углерод \(\left(\mathrm{CCl}_{4}\right)\), бензол, пропанол, этанол, ацетон.
Химические свойства
Салициловая кислота, будучи универсальной молекулой, может давать различные соединения для полезного использования после реакций.
Синтез аспирина
Ниже представлена схема реакции, которая использовалась для создания соединения. В этой реакции избыток уксусного ангидрида смешивают с известным количеством салициловой кислоты, а серная кислота служит катализатором. Уксусная кислота и ацетилсалициловая кислота (аспирин) создаются путем нагревания комбинации. Воду добавляют после процесса, чтобы удалить лишний уксусный ангидрид и вызвать кристаллизацию побочного продукта.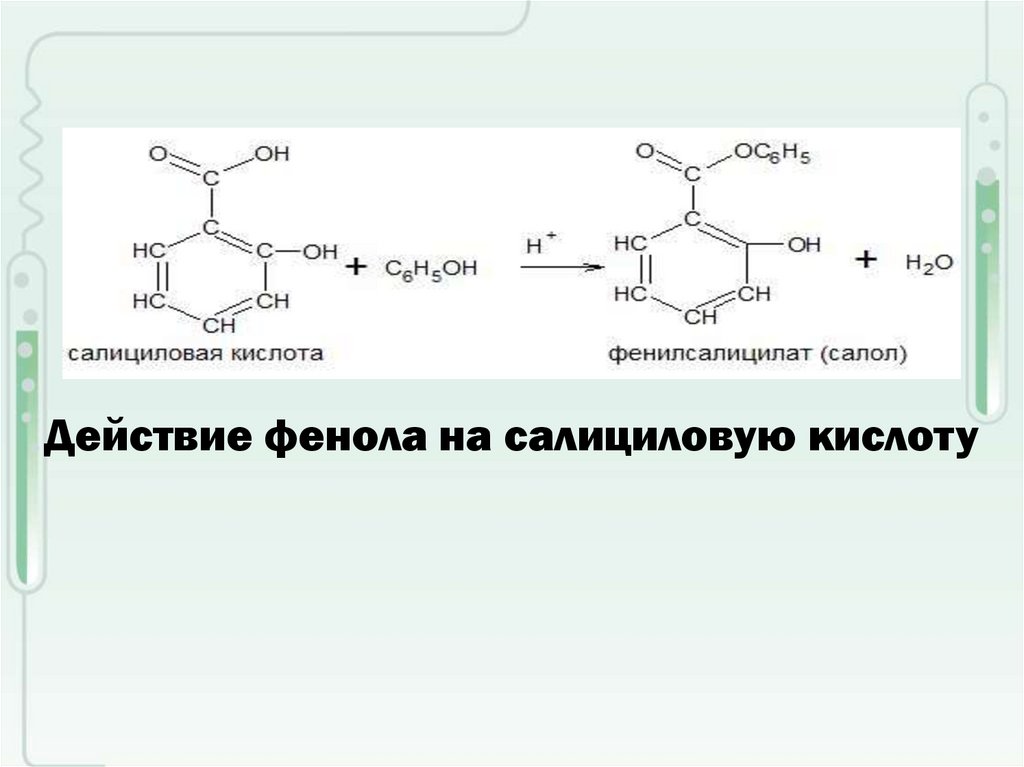 После сбора и перекристаллизации для очистки аспирин проверяется на температуру плавления.
После сбора и перекристаллизации для очистки аспирин проверяется на температуру плавления.
Реакция этерификации
Салициловая кислота является природной органической кислотой. Таким образом, он может объединяться с органической гидроксильной группой с образованием нового важного класса органических соединений, известных как сложные эфиры. Реакция дегидратации происходит при смешивании салициловой кислоты и метанола с нагреванием и кислой средой, предпочтительно серной кислотой. Эта реакция приводит к потере воды и образованию метилсалицилата. Карбоновая кислота теряет ион (-ОН-), присутствующий в молекуле салициловой кислоты. Кроме того, ион (H+) теряется в результате депротонирования молекулы метанола с образованием метилсалицилата (сложного эфира) и воды в качестве побочного продукта.
Побочные эффекты салициловой кислоты
Салициловая кислота представляет собой кератолитическое (отшелушивающее кожу) вещество, которое сбрасывает эпидермис кожи, вызывая кожные инфекции.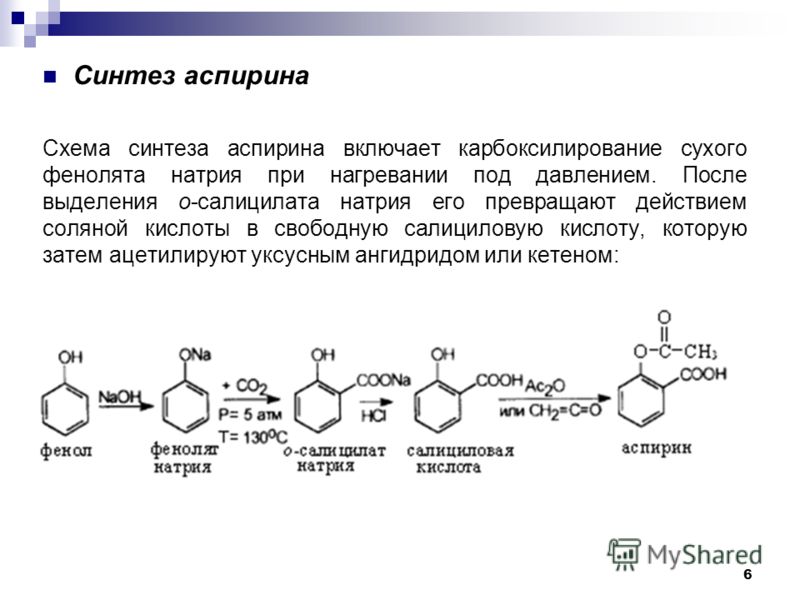 Более распространенными побочными эффектами являются раздражение кожи и жжение.
Более распространенными побочными эффектами являются раздражение кожи и жжение.
Симптомы передозировки
Спутанность сознания, потливость, шум в ушах, диарея, учащенное или глубокое дыхание, головная боль, потеря слуха, головокружение, тошнота, учащенное дыхание, звон или жужжание в ушах, сильная сонливость, дискомфорт в желудке и рвота являются некоторыми из симптомы, которые могут возникнуть.
Использование салициловой кислоты
Салициловая кислота имеет множество применений в различных областях:
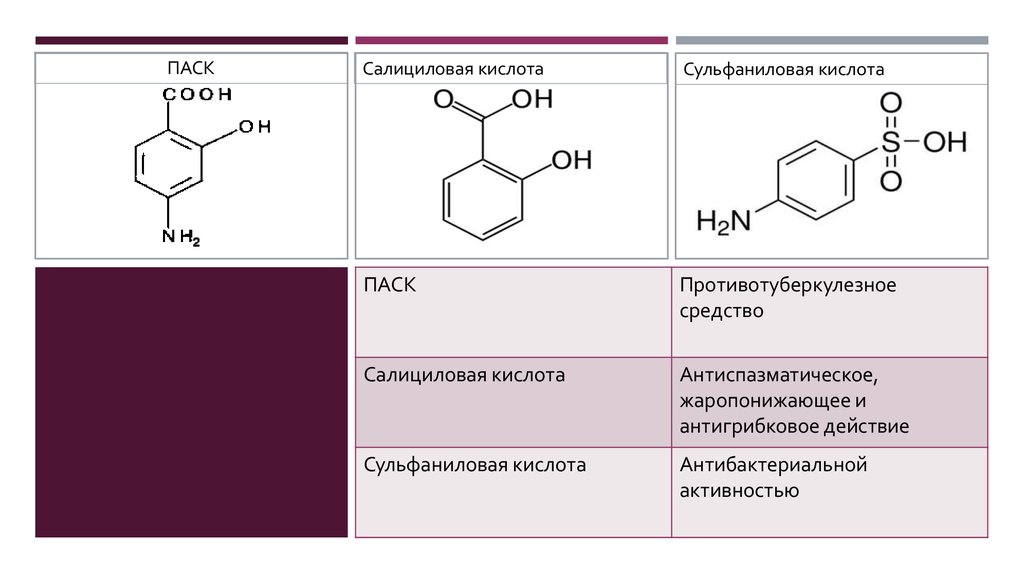
- Салициловая кислота используется во многих областях, особенно в фармацевтическом секторе. Салициловая кислота наиболее часто и широко используется в производстве обезболивающего аспирина, ацетилированного производного салициловой кислоты. Фармакологические достоинства салицилатов у людей имеют долгую историю.
- Аспирин (ацетилсалициловая кислота, полученная из салициловой кислоты) уменьшает боль, воспаление и отек суставов, предотвращая свертывание крови и защищая от сердечного приступа и инсульта.
- Салициловая кислота для местного применения (для кожи) используется для лечения состояний, включая псориаз, перхоть, себорею и акне, а также для избавления от бородавок, мозолей и мозолей.
- Метилсалицилат, эстерифицированное салициловой кислотой вещество, используемое в качестве анальгетика, также часто называют маслом грушанки. Этот анальгетик обычно лечит головные боли, боли и боли.
- Кератолитическое средство также может быть изготовлено из салициловой кислоты. Эти вещества используются для лечения различных кожных заболеваний и избыточного роста эпидермиса, самого внешнего слоя кожи, в виде химических отшелушивающих масок для кожи. Он служит инструментом для снятия кожи снаружи. Однако было бы очень хорошо, если бы человек принимал его только в соответствии с предписаниями вашего дерматолога, потому что у некоторых людей он может раздражать кожу, вызывая жжение, зуд и кожную сыпь.
- Кроме того, псориаз и акне лечат салициловой кислотой. Салициловая кислота осветляет кератиновый компонент кожи, разрывая межмолекулярные связи между двумя молекулами кератина, таким образом она лечит эти нарушения.
 Снижение его pH приводит к смягчению рогового слоя кожи. Он помогает при угревой сыпи, очищая закупоренные поры и сохраняя больше влаги, улучшая самочувствие и здоровье кожи.
Снижение его pH приводит к смягчению рогового слоя кожи. Он помогает при угревой сыпи, очищая закупоренные поры и сохраняя больше влаги, улучшая самочувствие и здоровье кожи. - Бородавки лечат салициловой кислотой. Его кератолитическая активность и то, как он лечит инфекцию бородавок, очень похожи. При введении он постепенно заставляет бородавки отделяться от тела, обезвоживая пораженные бородавками клетки кожи. Кроме того, началась небольшая воспалительная реакция, которая включает иммунологический ответ организма на вирусное заболевание бородавок.
- Одним из ингредиентов шампуней против перхоти является салициловая кислота. Салициловая кислота препятствует накоплению кожного сала в порах кожи и окружающих волосяных фолликулах, вот почему. Он помогает удалить шелушащиеся омертвевшие клетки кожи головы, предотвращая появление перхоти.
- Поскольку салициловая кислота является признанным бактериостатическим средством, она обладает слабым антисептическим действием.
 Вместо того, чтобы искоренять существующие микробы, он останавливает их развитие, где бы он ни использовался.
Вместо того, чтобы искоренять существующие микробы, он останавливает их развитие, где бы он ни использовался. - Кроме того, салициловая кислота способствует устранению черных и белых точек. Салициловая кислота делает это с помощью тех же процессов, что и профилактика акне. Он предотвращает закупорку пор кожи, а те, которые уже засорились, можно открыть, нанеся салициловую кислоту на это конкретное место. По сути, поры кожи забиваются, когда кератин откладывается в открытых фолликулах нашей кожи вместе с натуральным маслом, которое выделяет наша кожа. Благодаря своим кератолитическим свойствам салициловая кислота способствует расщеплению кератина, высвобождая закупоренные кожные фолликулы, поэтому их можно легко промыть водой.
Надеемся, вы хорошо поняли концепцию. Для четкого понимания и лучших результатов загрузите приложение Testbook сегодня для интерактивного концептуального обучения. Подготовьтесь к обучению с Testbook!
Часто задаваемые вопросы о салициловой кислоте
В. 1 Для чего используется салициловая кислота?
1 Для чего используется салициловая кислота?
Отв.1 В зависимости от лекарственной формы и интенсивности препарата салициловая кислота как лекарственное средство используется для диагностики ряда кожных заболеваний, включая акне, перхоть, псориаз, себорейный дерматит кожи и волосистой части головы , мозоли, мозоли, обыкновенные бородавки и подошвенные бородавки. 9{\circ} \mathrm{C}\)
Q.3 Какова формула салициловой кислоты?
Ответ 3 Формула \(\mathrm{C}_{6} \mathrm{H}_{4}(\mathrm{OH}) \mathrm{COOH}\)
Q .4 Какова молярная масса салициловой кислоты?
Ответ 4 Молекулярная масса салициловой кислоты составляет \(138,12 \mathrm{~g} / \mathrm{моль}\)
Q.5 Каковы источники салициловой кислоты?
Ans.5 В естественном состоянии растения вырабатывают салицилаты для защиты от токсичных веществ, включая патогены, грибки и насекомых.


