Sodium что это – что это такое, каковы вред и польза содиум\аммониум\магнезиум лаурет сульфат (sodium laureth\coco sulfate) и что значит «без sls»?
Sodium — это… Что такое Sodium?
| Натрий/Natrium (Na) | |
|---|---|
| Атомный номер | 11 |
| Внешний вид простого вещества |  серебристо-белый мягкий металл серебристо-белый мягкий металл |
| Свойства атома | |
| Атомная масса (молярная масса) | 22,989768 а. е. м. (г/моль) |
| Радиус атома | 190 пм |
| Энергия ионизации (первый электрон) | 495,6(5,14) кДж/моль (эВ) |
| Электронная конфигурация | [Ne] 3s1 |
| Химические свойства | |
| Ковалентный радиус | 154 пм |
| Радиус иона | 97 (+1e) пм |
| Электроотрицательность (по Полингу) | 0,93 |
| Электродный потенциал | -2,71 в |
| Степени окисления | 1 |
| Термодинамические свойства простого вещества | |
| Плотность | 0,971 г/см³ |
| Удельная теплоёмкость | 1,222 Дж/(K·моль) |
| Теплопроводность | 142,0 Вт/(м·K) |
| Температура плавления | 370,96 K |
| Теплота плавления | 2,64 кДж/моль |
| Температура кипения | 1156,1 K |
| Теплота испарения | 97,9 кДж/моль |
| Молярный объём | 23,7 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объемноцентрированая |
| Период решётки | 4,230 Å |
| Отношение c/a | n/a |
| Температура Дебая | 150,00 K |
| Na | 11 |
| 22,98977 | |
| 3s1 | |
| Натрий | |
Натрий — химический элемент с атомным номером 11 в периодической системе, обозначается символом Na (лат. Natrium), мягкий щелочной металл серебристо-белого цвета.
В воде натрий ведет себя почти так же, как литий: реакция идёт с бурным выделением водорода, в растворе образуется гидроксид натрия.
История и происхождение названия
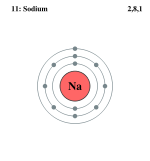
Схема атома натрия
Натрий (а точнее, его соединения) использовался с давних времён. Например, сода (натрон), встречающаяся в природе в водах натронных озёр в Египте. Природную соду древние египтяне использовали для бальзамирования, отбеливания холста, при варке пищи, изготовлении красок и глазурей. Плиний Старший пишет, что в дельте Нила соду (в ней была достаточная доля примесей) выделяли из речной воды. Она поступала в продажу в виде крупных кусков, из-за примеси угля окрашенных в серый или даже чёрный цвет.
Натрий впервые был получен английским химиком Хемфри Дэви в 1807 году электролизом твердого NaOH.
Название «натрий» (natrium) происходит от арабского натрун (по-гречески — nitron) и первоначально оно относилось к природной соде. Сам элемент ранее именовался содием (лат. Sodium).
Получение
Первым способом получения натрия стала реакция восстановления карбоната натрия углем при нагревании тесной смеси этих веществ в железной ёмкости до 1000°C:
Na2CO3+2C=2Na+3CO
Затем появился другой способ получения натрия — электролиз расплава едкого натра или хлорида натрия.
Физические свойства
Металлический натрий, сохраняемый в ксилоле
 Качественное определение натрия с помощью пламени — ярко-жёлтый цвет эмиссионного спектра «D-линии натрия», дублет 588,9950 и 589,5924 нм.
Качественное определение натрия с помощью пламени — ярко-жёлтый цвет эмиссионного спектра «D-линии натрия», дублет 588,9950 и 589,5924 нм.Натрий — серебристо-белый металл, в тонких слоях с фиолетовым оттенком, пластичен, даже мягок (легко режется ножом), свежий срез натрия блестит. Величины электропроводности и теплопроводности натрия достаточно высоки, плотность равна 0,96842 г/см³ (при 19,7° С), температура плавления 97,86° С, температура кипения 883,15° С.
Химические свойства
Щелочной металл, на воздухе легко окисляется. Для защиты от кислорода воздуха металлический натрий хранят под слоем керосина. Натрий менее активный чем литий, поэтому с азотом реагирует только при нагревании:
2Na + 3N2=2NaN3
При большом избытке кислодрода образуется перокcид натрия
2Na + O2 = Na2O2
Применение
Металлический натрий широко используется в препаративной химии и промышленности как сильный восстановитель, в том числе в металлургии. Натрий используется в производстве весьма энергоёмких натриево-серных аккумуляторов. Его также применяют в выпускных клапанах грузовиков как теплоотвод. Изредка металлический натрий применяется в качестве материала для электрических проводов, предназначенных для очень больших токов.
В сплаве с калием, а также с рубидием и цезием используется в качестве высокоэффективного теплоносителя. В частности, сплав состава натрий 12 %, калий 47 %, цезий 41 % имеет рекордно низкую температуру плавления −78 °C и был предложен в качестве рабочего тела ионных ракетных двигателей и теплоносителя для атомных энергоустановок.
Натрий так-же используется в газоразрядных лампах высокого давления ДНаТ (Дуговая Натриевая Трубчатая). Эти лампы очень широко применяются в уличном освещении. Они дают ярко-жёлтый свет. Срок службы ламп ДНаТ составляет 12-24 тысяч часов. Поэтому газоразрядные лампы типа ДНаТ незаменимы для городского, архитектурного и промышленного освещения.
Металлический натрий применяется в качественном анализе органического вещества. Сплав натрия и исследуемого вещества нейтрализуют этанолом, добавляют несколько милилитров дистиллированной воды и делять на 3 части, проба Ж. Лассеня (1843), направлена на определение азота, серы и галогенов (проба Бейльштейна)
Хлорид натрия (поваренная соль) — древнейшее применяемое вкусовое и консервирующее средство.
Азид натрия (Na3N) применяется в качестве азотирующего средства в металлургии и при получении азида свинца.
Цианид натрия (NaCN) применяется при гидрометаллургическом способе выщелачивания золота из горных пород, а также при нитроцементации стали и в гальванотехнике (серебрение, золочение).
Хлорат натрия (NaClO3) применяется для уничтожения нежелательной растительности на железнодорожном полотне.
Биологическая роль
В организме находится большей частью снаружи клеток (примерно в 15 раз больше чем в цитоплазме). Это разницу поддерживает натрий-калиевый насос, который откачивает попавший внутрь клетки натрий.
Совместно с калием натрий выполняет следующие функции:
- Создание условий для возникновения мембранного потенциала и мышечных сокращений.
- Поддержание осмотической концентрации крови.
- Поддержание кислотно-щелочного баланса.
- Нормализация водного баланса.
- Обеспечение мембранного транспорта.
- Активация многих энзимов.
Рекомендуемая доза натрия составляет для детей от 600 до 1700 миллиграмм, для взрослых от 1200 до 2300 миллиграмм. В виде поваренной соли это составляет от 3 до 6 грамм в день.
Натрий содержится практически во всех продуктах, хотя большую его часть организм получает из поваренной соли. Усвоение в основном происходит в желудке и тонкой кишке. Витамин Д улучшает усвоение натрия, однако, чрезмерно соленая пища и пища богатая белками препятствуют нормальному всасыванию. Количество поступившего с едой натрия показывает содержание натрия в моче. Для богатой натрием пищи характерна ускоренная экскреция.
Дефицит натрия у питающегося сбалансированой пищей человека не встречается, однако, некоторые проблемы могут возникнуть при вегетарианских диетах. Временный дефицит может быть вызвано использованием мочегонных, поносом, обильным потением или избыточным употреблением воды. Симптомами нехватки натрия являются потеря веса, рвота, образование газов в желудочно-кишечном тракте, и нарушение усвоения аминокислот и моносахаридов. Продолжительный дефицит вызывает мышечные судороги и невралгию.
Переизбыток натрия вызывает отек ног и лица, а так же повышеное выделение калия с мочой. Максимальное количество соли, которое может быть переработано почками составляет примерно 20-30 грамм, большее количество уже опасно для жизни.
См. также
Категория:Соединения натрия
Ссылки
| Электрохимический ряд активности металлов | |
|---|---|
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na | Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu, Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2, W, Sb, Bi, Ge, Re, Cu, Tс, Mn, Te, Rh, Po, Tl, Hg, Ag, Pb, Pd, Os, Ir, Pt, Au | |
| → активность металлов → |
Wikimedia Foundation. 2010.
Sodium hydroxide (Гидроксид натрия) в косметике. Что это такое, свойства, вред и польза, опасность для волос, кожи
Вещество Sodium hydroxide нередко используется в современной косметологии – косметике, ухаживающих и декоративных средствах для кожи и волос.
Содержание статьи:
Что это за вещество
Sodium hydroxide может носить разные названия: гидроксид или гидроокись натрия, каустическая сода или каустик. Едкий натр или едкая щелочь — еще одно наименование, которое ярко характеризует свойства вещества. Химическая формула вещества — NaOH.
Оно используется повсеместно в косметике и туалетных принадлежностях, в медицине и косметологии, в гражданской обороне, в пищевой, легкой и тяжелой промышленности. Гидроксид натрия представляет собой хлопьевидную субстанцию белого цвета, которая с легкостью абсорбирует воду.
 Sodium hydroxide
Sodium hydroxideВещество синтезируется из хлорида натрия. Вследствие своей щелочной природы, гидроксид натрия разъедает как органические вещества, так и металлы. Растворение в воде происходит на фоне выделения большого количества теплоты с получением гидратов.
Для чего его добавляют в состав косметики, полезные функции
Особенность Sodium hydroxide вступать во взаимодействие с маслами и образовывать соли натриевых жирных кислот обеспечивает основное действие вещества — омыление.
Свойства и функции у этого компонента в составе средств следующие:
- Sodium hydroxide в составе косметики регулирует уровень pH и снижает кислотность готового косметического средства.
- Компонент смывает грибковые и патогенные бактерии и создает защитный слой на поверхности кожи.
- Гидроксид натрия обладает обновляющим и антистатическим действием.
- В дерматологических препаратах используется для удаления бородавок и папиллом. При помощи средств с Sodium hydroxide размягчают и удаляют ороговевшие участки кожи.
- В составе кремов он оказывают на кожу увлажняющее действие, стягивают поры и удаляют отмершие клетки.
Есть ли от него вред и насколько сильный, опасность применения
Sodium hydroxide является агрессивным веществом, способным разлагать белки и липиды в коже, слизистых и других тканях, поэтому из-за риска дерматитов и реакций сенсибилизации в косметических средствах применяется дозировано. В низких концентрациях его применение безопасно для человека.

Обычно располагается в конце списка INCI из-за малой дозировки. В составе косметических средств он не обладает канцерогенностью и иммунотоксичностью, поэтому обычно не представляет опасности для применения женщинами в период беременности, может применяться в детской косметике для ухода за кожей.
В какой обычно косметике присутствует
Sodium hydroxide является поверхностно-активным веществом и входит в состав ухаживающих косметических средств. Популярный в косметологии глицерин содержит в составе гидроксид натрия. Компонент добавляют в мыло, шампунь, крем, скраб, зубную пасту, глазные капли, жидкую пудру и жидкость для снятия лака. Средства с гидроксидом натрия подходят для любого типа кожи.
Например, следующие косметические средства содержат его в своем составе:
- Garnier Чистая кожа — Гель + Скраб + Маска 3-в-1 с глиной;
- Rimmel London — Тушь для ресниц Scandaleyes XX-treme;
- Yves Rocher — Ночной крем anti-age global;
- Johnson&Johnson — Лосьон для тела «24 часа увлажнения» с миндальным маслом.
Запрещён ли он в разных странах?
Компонент Sodium hydroxide разрешен для производства косметических продуктов во всех странах с ограничениями по применению:
- косметическое средство должно использоваться только для кожи;
- гидроксид натрия должен входить в состав с учетом концентрации.
Правила и советы по применению косметики с этим веществом
Вещество гидроксид натрия в составе косметики не имеет каких-либо особенностей применения, поэтому следует ориентироваться на рекомендации по использованию конкретного продукта.
Щелочь Sodium hydroxide, находясь в свободном состоянии, вступает во взаимодействие с воздухом и водой, но в готовом продукте после реакции омыления она находится в связанном состоянии, поэтому косметические средства не требует особых условий хранения.
Поиск альтернативы
В качестве замены веществу, как моющим веществом может служить анионный ПАВ, произведенный из кокосового масла и кислоты — производной таурина. Он имеет пенообразующие свойства аналогичные лаурил-сульфату, но при этом изготовлен из природного сырья. Наименование в INCI: Sodium Lauroyl Methyl Isethionate.
Примером такого натурального пилинга может быть кокосовый скраб для тела производителя тайской косметики Banna. Другой натуральной заменой Sodium hydroxide выступает не омыляемый лецитин, полученного из сои (INCI: Behenyl alcohol Glyceryl stearate Phospholipids Glycine soja sterols). Этот натуральный эмульгатор снимает раздражение, питает и восстанавливает кожу.
Например, Pure Love ночной крем для лица с кислотами Омега 3 и Омега 6 (маслом черной смородины). Альтернативным моющим компонентом в шампуне может быть вещество алкилсукцинат (Sodium Lauroyl Methyl Isethionate). Пример мягкого шампуня на его основе — Klorane Nutri-Reparative with Desert Date.
В VII веке создали технологию мыловарения путем соединения гидроксида натрия с натуральными ароматическими маслами. Начиная с момента изобретения мыла и по сей день, очищающие и оздоравливающие свойства одновременно с безопасностью применения сделали Sodium hydroxide востребованным компонентом в современной косметике.
Видео о гидроксиде натрия
Мыло дома с нуля на гидроксиде натрия:
Автор: znaniesov
что это, функции в шампуне и вред
В списке ингредиентов ухаживающих и очищающих косметических средств постоянно используются поверхностно-активные вещества. Они направлены на глубокое очищение, растворение выделений сальных желез и отвечают за образование густой пены. Одним из таких веществ является Sodium Coco Sulfate. Что это за компонент, для чего применяется в продукции, и каков возможный вред для кожи и волос при регулярном использовании?
Химическое описание
Sodium Coco Sulfate — что это такое и для чего используется в косметической продукции? Данное вещество является активным компонентом для удаления загрязнений с поверхности кожи и волос. Он отвечает за образование густой очищающей пены при соприкосновении с водой для комфортного использования ухаживающей продукции. Производители косметики предпочитают добавлять Sodium Coco Sulfate в шампуни и другие средства, так как это один из самых дешевых поверхностно-очищающих компонентов. Он отлично растворяется в воде, но способен накапливаться в структуре волос и клетках кожи.

При ответе на вопрос о том, что это — Sodium Coco Sulfate, необходимо отметить, что данное вещество получают химическим путем из масла кокоса. Многих девушек данный факт вводит в заблуждение, так как масло кокоса является незаменимым помощником в уходе за сухими и поврежденными волосами. Но сульфаты — это продукты, которые имеют щелочную среду, а она наносит непоправимый вред красоте и здоровью.
Свойства
После того как стало понятно, что это — Sodium Coco Sulfate, необходимо обозначить основные характеристики вещества. Благодаря тому что их достаточно много, производители косметических продуктов добавляют его в список ингредиентов различных средств.

Основные свойства сульфатов:
- очень низкая стоимость;
- хорошие очищающие качества;
- абсорбируют жиры;
- сгущают консистенцию косметических средств;
- эффективно удаляют остатки ухаживающих и стайлинговых средств;
- образуют густую пену даже в комплексе с различными маслами;
- раздражают кожные покровы и слизистые оболочки;
- не утяжеляют волосы;
- позволяют легко наносить и смывать шампунь.
Вреда от Sodium Coco Sulfate гораздо меньше, чем от более агрессивных компонентов из группы сульфатов. Однако при регулярном применении и высокой концентрации он может вызывать большое количество проблем и дискомфорта.
Воздействие на кожу и волосы
Sodium Coco Sulfate в шампуне необходим для образования густой очищающей пены при соприкосновении с водой, а также для образования необходимой консистенции для комфортного использования косметического средства. Несмотря на то что данный компонент эффективно удаляет загрязнения, остатки стайлинговых средств, а также абсорбирует кожный жир, он способен вымывать естественный кератин и другие соединительные вещества. Поэтому вред Sodium Coco Sulfate в шампуне заключается в том, что при регулярном использовании волосы становятся ломкими, тусклыми, появляются секущиеся кончики.

В составе ухаживающих косметических средств для лица сульфаты играют очищающую роль. Но они способствуют тому, что необходимая влага быстро испаряется из клеток, кожа становится обезвоженной, склонной к шелушениям и сухости. Довольно часто при использовании косметики с Sodium Coco Sulfate обладательницы чувствительного эпидермиса могут заметить появление прыщей, покраснений и преждевременных морщин. Оттенок и состояние кожи заметно ухудшаются, что приводит к образованию неприятных ощущений и различных недостатков.

Многие дерматологи утверждают, что Sodium Coco Sulfate — это довольно опасное вещество, которое может проникать в глубокие слои кожи и волос и оставаться внутри долгое время. Поэтому при постоянном использовании шампуней с данным химических компонентом рекомендуется чередовать его с более натуральными ухаживающими продуктами.
Преимущества и недостатки
Несмотря на то что вред Sodium Coco Sulfate оспорить довольно сложно, данное вещество обладает рядом определенных преимуществ:
- эффективное и глубокое очищение;
- абсорбирование кожного жира;
- продление ощущения свежести и чистоты;
- образование густой пены;
- не утяжеляет волосы;
- бюджетная стоимость;
- имеет более вредные аналоги в данной группе компонентов.
Из недостатков можно выделить:
- пересушивание клеток кожи и волос;
- тусклость, ломкость, сечение при регулярном использовании;
- способствует образованию шелушений;
- может привести к возникновению аллергических реакций, зуда, сухости;
- раздражает кожные покровы и слизистые;
- преждевременное загрязнение и повышенная работа сальных желез;
- способен спровоцировать появление перхоти.
Поэтому перед тем как приобрести ухаживающие косметические средства, в составе которых присутствует данный компонент, необходимо тщательно подойти к вопросу выбора. Но на сегодняшний день на полках магазинов можно найти невероятный ассортимент продукции с абсолютно натуральным списком ингредиентов для бережного и безопасного ухода за кожей.
Чем заменяют сульфаты
Производители косметических средства все чаще переходят на использование натуральных ингредиентов, которые отлично выполняют все необходимые функции. Поэтому среди покупателей все более популярным становится шампунь без Sodium Coco Sulfate. Он мягко удаляет загрязнения, жиры, остатки всех косметических продуктов, не повреждает структуру и способен интенсивно напитать ее полезными компонентами.

Также можно без особого труда найти органические средства для очищения кожи лица и тела, которые не способствуют появлению шелушений и ощущения стянутости. Мировые дерматологи рекомендуют проверять составы всех косметических продуктов и искать там следующие компоненты:
Они являются более безопасными, но абсолютно не уступают по очищающим характеристикам вредным для красоты и здоровья сульфатам.
Заключение
Профессионалы в области дерматологии отмечают, что Sodium Coco Sulfate — это один из довольно вредных ингредиентов в составе косметических средств. Но благодаря его низкой стоимости многие производители добавляют его в шампуни, гели для тела и продукты для умывания. Перед покупкой специалисты рекомендуют тщательно проверять состав и отдавать предпочтение более натуральным и безопасным средствам.
Сульфат натрия — Википедия
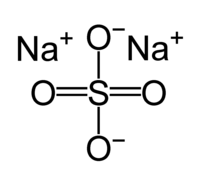
| Сульфат натрия | |
|---|---|
 ( {{{картинка}}}) | |
 ( ({{{изображение}}}) | |
| Систематическое наименование | сульфат натрия, натрий сернокислый |
| Хим. формула | Na2SO4 |
| Рац. формула | Na2SO4 |
| Состояние | белые гигроскопичные кристаллы |
| Молярная масса | 142,04 г/моль |
| Плотность | 2,68 г/см³ |
| Температура | |
| • плавления | 883 °C |
| Энтальпия | |
| • образования | −1387,9 кДж/моль |
| Растворимость | |
| • в воде | 19,2 (20 °C), 42,3 (100 °C) |
| Рег. номер CAS | 7757-82-6 |
| PubChem | 24436 |
| Рег. номер EINECS | 231-820-9 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E514(i) |
| RTECS | WE1650000 |
| ChEBI | 32149 |
| ChemSpider | 22844 |
| NFPA 704 |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Сульфат натрия, сернокислый натрий, Na2SO4 — натриевая соль серной кислоты.
Бесцветные кристаллы. Безводный Na2SO4 устойчив выше температуры 32,384 °C, ниже этой температуры в присутствии воды образуется кристаллогидрат Na2SO4·10H2O.
В природе безводный сульфат натрия встречается в виде минерала тенардита. Кристаллогидрат Na2SO4·10H2O образует минерал мирабилит (глауберову соль). Встречаются также двойные соли сульфата натрия с другими сульфатами, например астраханит Na2SO4·MgSO4·4H2O, глауберит Na2SO4·CaSO4. Значительные количества сульфата натрия содержатся в рапе и донных отложениях солёных озёр хлорид-сульфатного типа и заливе Кара-Богаз-Гол. В них при понижении температуры идёт реакция:
- 2NaCl + MgSO4 ⇆ MgCl2 + Na2SO4
В России крупнейшим производителем природного сульфата натрия является компания ОАО «Кучуксульфат» — 600 тыс. тонн в год.
Промышленный способ получения сульфата натрия — взаимодействие NaCl с H2SO4 в специальных «сульфатных» печах при 500—550 °C; одновременно получается хлороводород.
- 2NaCl+h3SO4⟶Na2SO4+2HCl{\displaystyle {\mathsf {2NaCl+H_{2}SO_{4}\longrightarrow Na_{2}SO_{4}+2HCl}}}
В настоящее время такой способ практически не используется, так как имеются достаточно большие запасы природного сырья.
Также сульфат натрия получается как отход (не имеющий запаха) в производстве хромпика.
В мире большое количество сульфата натрия использовались ранее при производстве синтетических моющих средств, однако во многих странах в последние годы произошёл переход на концентрированные (компактные) стиральные порошки, в которых сульфат либо не используется, либо используется в небольших количествах. В России производители стиральных порошков закупают более 300 тыс. тонн сульфата натрия.
Второе по количеству применение сульфата натрия — стекольное производство. Также это вещество используют в больших объёмах при получении целлюлозы сульфатным методом, а также в текстильной, кожевенной промышленности и в цветной металлургии.
В небольших количествах сульфат натрия находит применение в химических лабораториях — в качестве обезвоживающего средства. Несмотря на то, что он обезвоживает органические растворители медленнее, чем сульфат магния, многие предпочитают именно это средство по двум причинам: дешево и легко отфильтровывать.
В ещё меньших количествах ранее использовался в медицине и ветеринарии в качестве солевого слабительного средства и как компонент в средствах для промывания носа.
Зарегистрирован в качестве пищевой добавки E514.
Регулятор кислотности, используется как буферная добавка поддерживающая pH на определенном уровне [1].
Физиологическое действие и указания по технике безопасности[править | править код]
Сульфат натрия Na2SO4 пожаро- и взрывобезопасен. По степени воздействия на организм человека натрий сернокислый относится к IV классу опасности (малоопасные вещества) согласно ГОСТ 12.1.007-76. По токсикологии NFPA 704 сульфату натрия присвоена низшая токсичность.
- Реми Г. Курс неорганической химии. Т.2. — М., 1966

